1. 서론
2. 본론
2.1. AMR의 신속하고 정확한 진단
2.2. AI를 이용한 예측 기반 치료 결정
2.3. 의료기관 및 지역사회 차원의 항생제 관리에서의 AI의 역할
2.4. AI를 이용한 신약·신개념 항균제 설계
3. 결론
1. 서론
항생제 내성(antimicrobial resistance, AMR)은 인간·동물·환경을 아우르는 복합 요인이 맞물려 촉발되고 증폭되는 21세기 보건의 최대 난제 가운데 하나다. 가장 최근의 전 세계 규모의 분석에 따르면 2021년 단일 해에 박테리아 AMR과 연관된 사망은 약 471만 건(95% UI 4.23–5.19million), 이 중 114만 건(UI 1.00–1.28million)은 내성 자체에 직접 귀인되는 사망으로 추정된다 [1]. 특히 ESKAPE 병원체군(Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, Enterobacter spp.)은 치료 실패의 주요 원인으로 의료 체계에 심대한 부담을 주고 있다 [2,3]. 이러한 수치와 양상은 감염 치료가 현재에 머물러서는 안되며, 패러다임의 전환이 시급한 상황이다.
임상적으로 AMR은 치료 반응 지연, 사망률 증가, 의료비 상승, 입원 기간 연장 및 병원 내 전파 위험 상승을 통해 환자는 물론, 의료진과 의료체계를 동시 압박한다. 전통적으로 효과적이던 항생제가 점차 힘을 잃으면서 폐렴, 요로감염, 피부 및 연조직 감염과 같은 흔한 감염조차 치료가 어렵고 비용이 많이 드는 질병으로 변모하고 있으며, 이로 인해 수술, 장기이식, 항암치료 등 필수적 의료 절차의 안전성까지 위협받고 있다. 내성의 분자생물학적 및 역학적 양상도 갈수록 복잡해지고 있다. 다제내성균(MDR)과 치료가 어려운 병원체의 증가는 물론, 결핵처럼 배양과 감수성 검사에 오랜 시간이 걸리는 병원체에서도 약제 내성 예측과 치료 결정의 난이도가 높아지고 있다. 지역사회와 의료기관, 축산 및 환경 전반에 항생제 사용 빈도가 늘어날수록 내성균에게 유리한 선택압(selective pressure, 내성균이 살아남기 쉬운 압력(환경))이 커진다. 그 결과 수평적 유전자 전달(세균끼리 유전자를 주고받는 현상)과 이동성 유전요소(mobile genetic elements, eg. Plasmid)를 통한 내성 유전자가 사람-동물-환경의 경계를 넘나드는 문제로 진화하고 있으며, 이 문제는 “One Health” 관점에서 함께 다루어져야 한다 [4]. 또한 중국 국가감시망 자료의 카바페넴 내성 그람 음성균의 증가처럼, 지역·국가별 특정 내성이 가파르게 상승하는 경향도 확인된다 [5].
그러나 신약 개발 파이프라인은 이러한 속도를 따라가지 못하고 있다. 항균제 연구개발은 느리고 비용이 많이 들며 실패 위험이 크고, 임상적으로 의미 있는 새로운 기전의 항생제 등장은 드물다. WHO가 발간한 2023년 ‘임상 및 전임상 개발 중인 항생제 보고서(Antibacterial agents in clinical and preclinical development)’에 따르면, 2017년 7월 1일부터 2023년 12월 31일까지 13개의 새로운 항생제만이 판매 승인을 받았으나, 그중 단 2개만이 신규계열로 분류되어 새로운 항생제의 공급부족 및 혁신성 결핍의 문제는 지속되고 있는 실정이다 [6,7]. 항생제 개발의 쇠퇴 추세는 이미 2010년대 이전부터 지적되어 왔으며, 현존 항생제로 AMR을 효과적으로 제어하기에는 역부족이라는 경고가 거듭되어 왔다 [8,9].
이러한 위기 속에서 인공지능(Artificial Intelligence, AI)과 머신러닝(Machine Learning, ML)은 AMR 대응 전 주기에 걸쳐 ‘데이터에서 결정으로(From data to decisions)’를 가속하는 핵심 도구로 부상했다 [10], [그림 1]. AI/ML은 전자의무기록, 미생물검사, 유전체, 지역 내성 동향 등 이질적 데이터를 통합 분석하여 병원체 동정하고 내성 예측 및 치료 반응 예측을 고도화하고, 환자 맞춤형 항생제 선택 및 용량, 치료 기간을 제안하는 임상결정지원시스템(Clinical decision support systems, CDSS)을 통해 처방의 질을 높일 수 있다. 실제로 matrix assisted laser desorption ionization-time of flight mass spectrometry (MALDI TOF)와 같은 새롭게 개발된 기술과 ML의 결합은 내성 예측 시간을 단축시켜 환자의 89%에서 항생제 요법 변경 가능성을 시사했고 [11], UTI용 CDSS는 불필요한 광범위 항생제 사용 경향을 낮추고 1차 약제 원칙 준수를 촉진하였다 [12]. 또한 원격의료 환경에서도 항생제 관리의 지침 부합률이 대면 진료를 능가하는 결과가 보고되었다(92.5% vs 90.7%) [13].
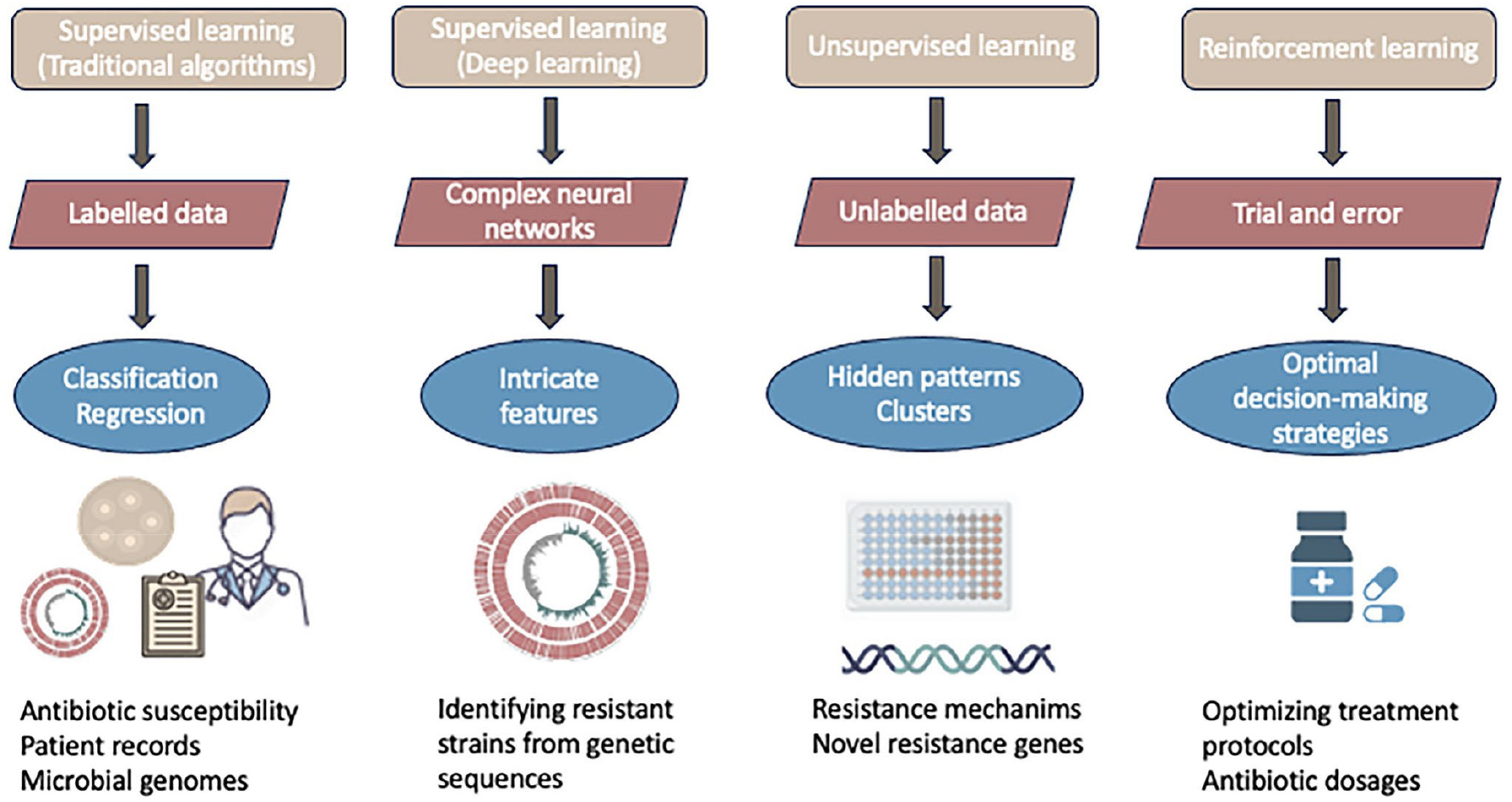
그림 1.
항생제 내성(AMR) 문제 해결에 활용되는 머신러닝(ML) 방법과 그 적용 분야 [10].
(1) 지도 학습(Supervised Learning) : 레이블이 지정된 데이터를 사용해 모델을 훈련하는 방법으로 정답이 있는 데이터를 활용해 패턴을 학습한 뒤, 새로운 데이터의 결과를 예측하는 데 사용된다. 전통적 알고리즘(Traditional algorithms)은 대표적으로 환자 기록이나 미생물 유전체 등 정형화된 데이터를 분석해 항생제 감수성을 예측할 수 있고, 딥러닝(Deep learning)은 복잡한 신경망을 활용해 유전체 염기 서열과 같은 복잡하고 비정형적인 데이터에서 저항성 균주를 식별하는 데 이용될 수 있다. (2) 비지도 학습(Unsupervised Learning) : 레이블이 없는 데이터를 분석해 숨겨진 패턴이나 그룹(클러스터)을 찾아내는 방법으로 저항성 메커니즘을 이해하거나 새로운 저항성 유전자를 발견하는 데 사용될 수 있다. 예를 들어, 특정 유전적 특성을 공유하는 균주들을 묶어 새로운 내성 클러스터를 파악할 수 있다. (3) 강화 학습(Reinforcement Learning) : 시행착오를 통해 최적의 결정을 내리도록 알고리즘을 훈련하는 방법으로 항생제 치료 전략이나 약물 조합을 최적화하여, 환자 반응을 기반으로 적절한 항생제 용량이나 치료 기간을 결정하는 모델을 개발할 수 있다(치료 프로토콜의 최적화).
예측 정확도의 측면에서도 유전체 표현형 데이터를 학습한 ML 모델들은 특정 병원체·항생제 조합에서 90%를 상회하는 정확도를 보고하며(예: Pseudomonas aeruginosa, Staphylococcus aureus 혈류감염 내성 예측), 표준 감수성 검사보다 더 빠른 시간 내에 임상적으로 유의한 정보를 제공할 잠재력을 입증해 왔다 [14,15,16]. 뿐만 아니라, 항생제 사용의 적시성, 적정성을 높이는 AI 기반 항생제 관리 전략은 실제 진료 현장에서 잘 작동할 뿐 아니라, 여러 의료기관과 지역사회, 원격진료 환경으로도 쉽게 확장할 수 있게 발전하여 불필요한 광범위제제 사용 감소, 약물 전환/중단 판단의 보조 등 실제 진료 흐름에 안정적이고 효과적인 개입으로 확장되고 있다 [17]. 또한 신규 항균제 발굴에서도 AI의 파급력은 뚜렷한데, AI 주도 항균제 탐색의 방법론, 재현성, 오픈사이언스 구현은 전임상 가속화의 중요한 단계로 부상하고 있어, 데이터 품질 및 설명가능성, 외부 검증을 핵심 원칙으로 하는 새로운 연구 생태계 구축이 요구된다 [18].
끝으로, AMR은 본질적으로 One Health 문제로 인식해야 하는데, 너무나 많은 고려사항과 방대한 Data가 문제 인식과 해결 방안 모색에 어려움으로 지적되어 왔다. AI는 사람·동물·환경 데이터를 가로지르는 대규모 이종 데이터를 수집하고 연계해 해석을 돕고, 항생제 사용의 농축 지점(의료, 축산, 폐수 등)과 노출 경로를 정량화하여 위험지도를 제시함으로써, 예방 감시 개입의 선순환을 가능하게 할 수 있다. 본 종설은 AMR의 임상적 부담과 파이프라인의 위기를 직시하되, AI가 제공하는 실용적 해법 – 신속하고 정확한 진단, 예측 기반 치료 결정, 병원 및 지역사회 차원의 항생제 관리, 그리고 신약·신개념 항균제 설계 등을 소개하고, 임상 현장, 특히 요로감염을 포함한 비뇨의학적 감염에서 구현 가능한 AI의 이용을 알아보고자 한다.
2. 본론
2.1. AMR의 신속하고 정확한 진단
감수성 검사(AST)는 통상 24–72시간이 소요되어 광범위 항생제의 경험적 사용 기간이 길어지기 쉽다. 빠른 병원체 동정과 내성 예측은 초기 처방의 정확도를 높이고, 불필요한 광범위제 사용을 줄이는 것이 핵심이다. 최근 도입된 영상기반 신속 AST 플랫폼과 AI/ML 기반 예측 모델은 보고 시간을 수 시간대로 단축하며, 진료 흐름과 항생제 관리(Antimicrobial Stewardship, AMS)를 동시에 개선할 수 있는 수단으로 부상하고 있다. 즉, AI 기반 신속 진단 도구가 환자 치료를 더 빠르고 정확하게 할 뿐 아니라, 병원 전체의 항생제 사용을 체계적으로 관리하는 데에도 도움이 될 수 있다. 혈류감염 환자에서 사용하는 Accelerate Pheno™ 시스템은 혈액배양에서 균이 자라면 바로 분석을 시작해, 약 7시간 안에 세균의 종류(organism identification, ID)와 어떤 항생제에 듣는지(antibiotic susceptibility testing , AST)를 동시에 알려준다. 기존의 전통적인 검사에서는 결과가 나오기까지 보통 2~3일이 걸리는데, 이 장비는 보고 시간을 하루 이상 앞당겨 의사가 더 빨리 적절한 항생제를 선택할 수 있게 돕는다 [19,20,21].
임상에서 흔히 사용하는 MALDI-TOF 장비는 세균의 단백질 패턴을 분석해 균의 종류를 빠르게 알려준다. 최근에는 여기에 머신러닝(ML) 기술을 결합해, 균을 확인하는 동시에 어떤 항생제에 잘 듣고, 어떤 항생제에는 내성이 있는지도 예측하려는 시도가 활발하다. 대표적인 연구로 Weis 등은 실제 환자에서 얻은 30만 건이 넘는 MALDI-TOF 스펙트럼 데이터와 항생제 내성 정보를 학습시켰다. 그 결과, 특정 세균과 항생제 조합에서 매우 높은 정확도(AUC 값)로 내성을 예측할 수 있었다. 연구자들이 과거 환자 기록을 다시 분석해보니, 이런 결과를 진료에 활용했을 경우 약 89%의 환자에서 항생제 처방을 바꿀 수 있었을 것으로 나타났다 [22]. 즉, 기존의 배양 기반 감수성 검사가 나오기까지 며칠 기다릴 필요 없이, 균 동정 단계에서 곧바로 내성 여부를 예측할 수 있는 가능성이 입증된 것이다. EMBO Molecular Medicine의 Khaledi 등(2020)은 414개의 Pseudomonas aeruginosa 균주의 유전체 정보(유전자 서열)과 전사체 정보(유전자 발현 패턴)을 학습시켰고, 그 결과, 특정 항생제에 대한 내성을 예측할 때 정확도가 0.9를 넘는 경우도 있을 정도로 높은 성능을 보고하였다 [23]. 즉, 이 연구는 “세균이 실제로 항생제에 잘 듣는지(표현형 감수성)”를 직접 배양 검사로 확인하기 전에, 유전자와 발현 패턴(분자적 표지)을 조합해 미리 예측할 수 있다는 가능성을 보여준 것이다. Wang 등은 혈류감염을 포함한 466개 Staphylococcus aureus 임상 균주의 전장유전체(Whole Genome Sequencing) 데이터를 세분화된 유전자 단편(k-mer, 유전체 서열을 길이가 k인 짧은 염기서열 조각으로 잘라 분석하는 방법) 단위로 분석하고, 이를 머신러닝 알고리즘에 학습시켰고 그 결과, 여러 항생제에 대해 세균이 감수성(susceptible), 중간(intermediate), 내성(resistant)인지 분류하는 정확도가 90% 이상으로 나타났다고 보고하였다 [24]. 더 나아가, 이 방법은 표준 감수성 검사(AST)보다 약 6시간 빨리 결과를 제공할 수 있는 가능성을 보여주었다. QMAC-dRAST (QuantaMatrix, Seoul, Korea)는 미세유체 칩 기술(microfluidic chip technology)을 이용해 세균의 성장 반응을 관찰하는 방식으로 항생제 감수성 검사가 가능하다. 이 장비는 혈액배양이 양성으로 나온 직후 검체를 이용해, 보통 이틀 이상 걸리는 결과를 평균 6시간 만에 알려줄 수 있다. 2024년 연구에서는 기존의 표준 검사법과 비교했을 때, Categorical Agreement(항생제 감수성/내성 판정의 일치율)이 92.5%, Essential Agreement(MIC 수치 차이가 허용 범위 내에서 일치한 비율)이 89.0%로 보고되었다 [25]. 또 다른 연구에서는 그람음성균을 대상으로 VITEK 2와 비교했는데, 이때도 빠른 속도와 충분한 정확성을 확인한 바 있다 [26]. 무엇보다 국내에서 개발된 장비라는 점은 실제 병원 현장에 도입하고, 검사실 인력을 교육하고 운영함에 실용성이 높을 것으로 기대되며 궁극적으로는 패혈증 환자에서 초기 항생제를 더 빨리 바꿀 수 있도록 도와주는 도구가 될 수 있을 것으로 기대된다. 이러한 연구들은 모두 배양검사를 기다리지 않고도, 유전자 정보와 AI를 활용해 감수성을 빠르게 추정할 수 있는 새로운 진단 틀을 제시한 시도라고 할 수 있다.
비뇨의학과 질환과 관련된 연구들을 살펴보면, 복잡성 요로감염(cUTI) 환자를 대상으로 한 연구에서는 해석 가능한 머신러닝 모델을 이용해 항생제 내성 위험을 예측하였다 [27]. 이를 통해 퀴놀론이나 3세대 세팔로스포린 같은 항생제를 무분별하게 쓰는 일을 줄이고, 초기 경험적 치료에서 부적절한 처방을 예방할 수 있음을 보여주었다. 특히 외래나 응급실 상황에서 환자의 동반질환, 최근 항균제 사용력, 지역 내성률 등의 정보를 종합해 내성 위험을 조기에 예측한다면 실제 진료에서 큰 도움이 된다. 또 다른 연구에서는 LAMP (Loop-mediated isothermal Amplification, DNA 증폭법의 일종으로, 특정 유전자를 빠르고 간단하게 복제하는 기술)와 스마트폰 기반 머신러닝 판독 플랫폼을 이용해 ESBL이나 카바페넴분해효소 같은 내성 유전자를 1시간 안에 검출할 수 있었으며, 민감도와 특이도 모두 95% 이상으로 보고되었다 [28]. 이러한 방법은 소변 등 요로계 검체에서 복잡한 장비나 숙련된 전문 인력 없이도 사용할 수 있어, 비뇨의학과의 가까운 진료 현장에서 바로 적용할 수 있는 “near-patient” 진단 도구로 발전할 가능성을 보여준다.
AI를 이용한 항생제 내성 진단의 성능은 어떤 균주인지, 어떤 항생제인지, 또 학습에 사용된 데이터의 질이 얼마나 좋은지에 따라 달라진다. 하지만 아직까지는 외부 기관에서 검증한 연구가 부족하고, 보고된 결과도 연구마다 차이가 크다는 문제가 있다. 또한 WGS(전장유전체)나 오믹스(omics) 기반 모델(세균이 가진 유전자부터 실제 작동 결과물(단백질, 대사산물)까지를 전체적으로 분석하여 특정 세균이 어떤 항생제에 민감한지, 내성이 있는지를 예측하는 모델)은 검사 비용이 많이 들고, 결과가 나오기까지 걸리는 시간(TAT, Turn around time)이 길며, 의사가 이해하고 활용하기엔 아직 복잡하다. 영상 분석이나 라만 분광 기반 기술(Raman spectroscopy: 세균에 빛-레이저를 조사하여 빛의 일부가 세균 분자와 상호작용해서 발휘하는 특정한 패턴(라만 스펙트럼)을 AI/ML을 이용하여 분석하여 세균의 항생제 내성 여부를 빠르게 예측하는 방법)도 정확성과 속도는 뛰어나지만, 임상에서 쓰려면 검사 방법을 표준화하고 자동화하는 과정이 더 필요하다.
최근까지도 제시되고 있는 AI 임상 적용의 가장 큰 한계와 문제점은, 데이터의 질 부족, 표준화 미흡, 결과 해석의 어려움, 실제 임상환경에서의 불확실성이라고 할 수 있다 [29]. 따라서 이런 기술을 실제 환자 진료에 도입하려면, 전향적 연구를 통한 검증, 실제 진료 워크플로에 통합하는 시험, 그리고 정기적인 성능 재평가가 반드시 필요하다.
2.2. AI를 이용한 예측 기반 치료 결정
예측 기반 치료 결정은 환자별 자료(최근 배양 검사 결과, 항생제 노출 이력, 병력이나동반질환, 활력징후, 기초검사, 지역 및 병원 내 내성률 정보 등)를 머신러닝(ML) 모델에 입력해 항균제별 유효(감수성) 확률을 산출하고, 그 확률을 바탕으로 경험적 1차 약제 선택, 탈에스컬레이션(De-escalation: 광범위 항생제로 치료를 시작했다가, 원인균과 감수성 결과가 확인되면 더 좁은 범위 항생제로 바꾸는 것), 경구 전환 및 항생제 조기 중단 시점을 정교하게 결정하는 접근이다. 최근 문헌들은 AI/ML이 외래와 입원 영역 모두에서 항생제 선택의 정확도와 스튜어드십 성과(광범위제 감소, 부적절 치료 감소 등)를 향상시킬 잠재력을 반복적으로 제시한다 [10,17]. 임상 적용을 위해서는 해석 가능성(Interpretability : AI나 머신러닝 모델이 왜 그런 예측이나 권고를 했는지 사람이 이해할 수 있게 설명해 주는 능력), 데이터 표준화, 외부 검증이 중요하다는 점도 일관되게 지적된다.
외래 또는 응급실에서 요로감염의 경험적 치료는 환자별 내성 위험을 수치화해 “좁은 범위이지만 유효할 확률이 높은” 1차 약제를 우선 제시하는 전략이 핵심이다. Kanjilal 등의 의사결정 알고리즘은 전자의무기록(EHR)만으로 약제 비감수성 확률을 계산해, 후향 평가에서 2차선(광범위) 항생제 사용을 67% 줄이고, 동시에 부적절 치료를 18% 감소시켰다 [12]. 요점은 “안전하게 좁힐 수 있는 환자를 가려내어” nitrofurantoin, TMP SMX 같은 1차 약제를 더 자주, 근거 있게 쓰게 만든다는 데 있다. Yelin 등은 10년간 70만건 이상의 UTI와 500만건 이상의 개인별 항생제 구매 기록을 연결해, 과거 소변배양검사, 약제 구매 이력이 내성의 강력한 예측인자임을 보여주었고, 이 정보를 활용한 알고리즘이 경험적 치료의 불일치(내성 약제 처방) 위험을 유의하게 낮출 수 있음을 보였다 [30]. Yang 등은 복잡성 요로감염(complicated UTI)에서 해석가능 ML을 사용해 nitrofurantoin, co-trimoxazole, ciprofloxacin, levofloxacin 등의 내성 위험을 예측하고, 모델이 어떤 특징(최근 항생제 노출, 카테터, 당뇨, 지역 내성률 등) 때문에 그런 권고를 내렸는지 설명하여 임상의의 수용성을 높였다 [31]. “개인화된 항생제감수성표(personalized antibiogram)”라는 개념은 환자 개인의 과거 배양 결과, 최근 항생제 사용 이력, 지역 내성률 같은 정보를 합쳐서 그 환자에게 맞는 항생제 효과 예측표를 만들어 주는 것이다. 기존에는 병원 전체나 지역 단위에서 만든 평균적인 antibiogram을 참고했지만, 개인별 위험도는 달라서 실제 처방과 맞지 않는 경우가 많았다. STAnford Research Repository (STARR) clinical data(2009년 1월-2019년 12월)를 이용한 연구에서는, 이 개인화된 예측표를 적용했을 때 90.4%에서 항생제가 실제로 균에 효과적이었고, 이는 같은 상황에서 임상의가 직접 선택한 경우의 88.1%보다 더 높은 정확도였다 [32]. 즉, 환자별 맞춤 antibiogram을 활용하면 광범위제를 덜 쓰면서도 충분히 효과적인 항생제를 선택할 수 있다는 점이 입증되었다고 할 수 있다. 이러한 근거들은 외래나 응급실에서 요로감염 환자를 처음 진료할 때, 환자에게 꼭 필요한 항생제를 빠르고 정확하게 선택하는 데 큰 도움을 줄 수 있다.
입원 환자에서의 치료 과정 결정(탈에스컬레이션, 경구 전환, 항생제 조기 중단)에서도 AI는 실무적 가치를 보인다. Bolton 등은 중환자실 환자들의 데이터를 바탕으로 AI 모델을 이용해 시간의 흐름에 따라 변화하는 데이터를 분석하고 중요한 특징을 추출하여 가상의 시나리오 - “만약 오늘 항생제를 중단한다면”과 “계속 투여한다면” 두 가지 가정에서 환자의 결과가 어떻게 달라질지를 가상으로 비교했다 [33]. 그 결과, 항생제를 조금 일찍 중단하더라도 환자의 사망률에 유의한 차이는 보이지 않았고, 평균 입원 기간은 약 2.7일 줄어들었다. 또한 폐렴과 요로감염(UTI) 환자 데이터를 대상으로 한 분석에서도 항생제를 더 짧게 사용했을 때 입원 기간이 단축되는 긍정적 효과를 확인하여 더 짧은 치료가 더 긴 치료에 비해 열등하지 않다는 기존의 임상 연구 결과와 일치한다. 이러한 발전은 의료진이 데이터 기반의 합리적인 결정을 내릴 수 있도록 지원하여 불필요한 항생제 사용을 줄이고 항생제 내성 문제 해결에 기여할 수 있을 것이다.
학습되는 데이터와 AI/ML 알고리듬이 정교화되고 고도화 된다면, 진료 시점에 환자의 배양검사 결과, 항생제 노출 이력, 비뇨기계 시술력(수술 및 입원, 도뇨관이나 요관부목 삽입 이력 등)을 자동 수집해 항균제별 유효 확률과 함께 권고되는 항생제를 제시하여 수용성을 높일 수 있을 것이다. 또한 72시간 재평가에서 탈에스컬레이션, 경구전환, 중단을 각각의 예측 카드로 시각화해 팀 협진(감염내과, 약제, 간호)에서 공유하고 다양한 성과 지표(2차선 항생제(second- line antibiotics) 비율, 부적절 치료율, DOT (Days of Therapy: 항생제를 환자에게 투여한 “일수”를 의미), 7일 재내원, CDI (Clostridioides difficile Infection)발생 등)를 비교하고 모니터링하여 임상 성과를 향상시키고 항생제 내성에 발현에 대응할 수 있을 것이다 [17,34]. 앞으로의 AI를 이용한 감염병 진료의 발전 방향은 비교적 명확하다. (1) 특정 개인의 antibiogram을 표준 antibiogram 상에서 분석하여 환자 특이적 위험도를 기반으로 요로감염 진료 시 1차 약제 원칙을 강화한다. (2) 치료 전-중–후의 연속 의사결정(시작 약제 선택 → 48–72시간 탈에스컬레이션 및 경구 전환 → 종료)을 하나의 모델로 연결해 “누구에게·무엇을·언제까지”를 예측한다. (3) 설명가능 ML을 기반으로 편향(성별·연령·기저질환) 점검, 기관 간 외부 검증, 국내 항생제 내성률 및 의사 처방 경향 반영 등 알고리듬 고도화를 병행해야 한다. 궁극적으로, 이러한 AI의 이용 체계가 광범위 항생제 사용 및 처방 기간 최소화와 임상 안전성의 균형을 이끌어내 요로감염 진료의 질을 향상 시킬 수 있을 것이다.
2.3. 의료기관 및 지역사회 차원의 항생제 관리에서의 AI의 역할
전자처방(computerized provider order entry, CPOE) 화면에 환자별 다제내성균(multidrug-resistant organisms, MDRO) 위험 추정치를 실시간으로 보여주고(CPOE prompts) 저위험 환자에게는 표준 스펙트럼 약제를 권고하는 시스템의 효과가 무작위 다기관 시험에서 입증되었다 [35,36]. INSPIRE‑UTI RCT [36]에서는 CPOE prompts 사용균이 입원 1–3일 동안 광범위 항생제 DOT을 17.4% 줄였고, 중환자실 전실, 재원일수 등 안전성 지표에는 유의미한 차이가 없었다. 같은 방식의 INSPIRE Pneumonia RCT [36]에서도 광범위 항생제 DOT 28.4% 감소가 재현되었다. 이 연구들의 요지는 실시간 위험 예측과 추천 프롬프트를 사용하고 이를 교육에 반영하면 초기 경험적 처방에서 광범위제 남용을 줄이고 표준 약제 사용을 늘릴 수 있다는 점이다. 이러한 접근은 시스템만 갖추어진다면 입원 환자의 요로감염에도 그대로 적용 가능하며, 입원 초기에 ‘기본 약제부터’ 사용하도록 유도하여 항생제 선택의 원칙을 지키게 하는 의료기관 차원의 시스템으로서 유효하다.
병원에서 시행하는 Prospective Audit & Feedback(PAF, 처방 사전검토와 피드백)은 항생제 관리에 효과적이지만, 모든 항생제 처방을 전부 확인하려면 많은 인력과 자원이 필요하다. 미국의 한 대형 병원에서는 실제 처방 데이터를 바탕으로 ASP (Antimicrobial Stewardship Programs) 개입이 필요한 처방을 예측하고, 검토를 생략해도 안전한 처방을 식별하는 모델을 만들어, 개입이 필요하지 않을 가능성이 높은 처방은 자동으로 걸러내는 방식을 적용했다. 그 결과, 검토해야 할 건수를 절반 가까이(49%) 줄이면서도 필요한 처방은 78% 이상 놓치지 않았다. 또, 복잡한 모델이 아니더라도 ASP 개입이 필요한 처방을 높은 정확도로 식별하면서도, 검토가 필요한 전체 처방 건수를 상당히 줄일 수 있었다 [37]. 이 연구는 항생제 사용 관리에 AI와 머신러닝을 접목했을 때 얻을 수 있는 구체적인 임상적 의미를 보여준다. 병원의 ASP 팀이 모든 항생제 처방을 일일이 검토하지 않아도, 머신러닝 모델이 개입이 필요한 핫스팟(hotspot)을 효율적으로 찾아내어 인력과 자원을 절약할 수 있었다. 또한 특정 항생제(예: 플루오로퀴놀론)나 특정 상황(예: 임상 약사가 없는 병동)에서 개입 가능성이 높다는 모델의 예측은, 의료진에게 맞춤형 교육이나 표적화된 피드백을 제공하는 데 활용될 수 있다. 결국 AI를 활용하면 한정된 인력으로도 더 많은 고위험 처방을 신속히 검토하고, 실제 ASP 개입이 필요한 부적절 처방을 효과적으로 식별할 수 있다. 이를 통해 환자에게 보다 적절한 항생제를 투여하고 불필요한 항생제 노출을 줄임으로써, 궁극적으로 항생제 내성(AMR) 위험을 낮출 수 있을 것으로 기대된다.
입원 중인 환자에서 항생제 치료의 중단시점을 정하는 것은 매우 중요하다. AI가 “항생제 투여를 조기에 중단할지, 계속할지” 두 시나리오로 가정해 비교한 연구를 살펴보면, 조기 중단을 택했을 때 평균 재원기간이 2.71일 짧아졌고, 사망률의 유의미한 차이는 없었다 [33]. 즉, AI가 ‘언제 끊어도 안전한지’ 판단을 도와 불필요한 연장을 줄일 수 있었다. 또 다른 연구는 항생제의 정맥투여에서 경구투여(IV→PO) 전환 시점을 환자별로 공정하고 해석 가능하게 예측하는 모델을 제시했다 [38]. 이 연구의 요지는 특정 환자가 언제 경구용 항생제로 전환해도 안전한가를 데이터로 보여 주어, 경험적 규칙을 표준화된 근거로 바꾸는 데 ML기반 임상 의사결정 지원 시스템(clinical decision support system)이 도움이 될 수 있다는 점이다. 추후 전향적 안전성 평가가 필요하지만 이런 AI 및 ML 기반 알고리즘을 입원 48–72시간 재평가에 도입하면, 항생제 사용일수(DOT) 단축, 광범위 항생제(2차선) 처방 비율 감소, CDI 억제 같은 스튜어드십 지표 개선으로 이어질 가능성이 크다. 최근 문헌도 AI가 항생제 선택·사용을 개선할 잠재력을 지지하면서, 외부검증과 표준화, 설명 가능성의 중요성을 강조하고 있다 [39].
지역사회와 외래 진료에서는 AI를 이용한 개인화 예측과 원격의료 기반의 ASP가 핵심 역할을 한다고 할 수 있다. Kanjilal 등은 단순 요로감염(UTI) 환자에서 머신러닝(ML) 의사결정 알고리즘을 광범위 항생제 사용은 줄이면서도 치료 성공률(커버리지)은 유지할 수 있도록 설계하여 검증하였다 [12]. 이 연구는 항생제 내성 문제와 관련하여, 경증의 요로 감염에도 불구하고 광범위 항생제(Fluoroquinolone)가 흔히 처방되는 현실을 다루고 있다는 점에서 시사점이 크다. 저자들은 1만 명 이상의 환자 EHR (electronic health record)을 바탕으로 기계 학습 모델을 구축하여, 특정 항생제에 대한 세균의 감수성을 예측하고 이를 가장 좁은 스펙트럼의 항생제 처방을 권장하는 알고리즘으로 발전시켰다. 3,629명의 환자를 대상으로 이 알고리즘을 후향적으로 테스트한 결과, 광범위 항생제(second-line antibiotics, 2차선 항생제) 사용이 67% 감소했다. 또한 세균이 내성을 가진 항생제를 처방하는 부적절한 치료가 18% 감소했다. 비슷한 맥락에서, ML을 이용한 “개인 맞춤형 항생제 감수성표(personalized antibiograms)”는 환자의 과거 병력, 최근 감염·항생제 사용 이력 등을 반영해 “이 환자에게 가장 효과적일 가능성이 높은 항생제는 무엇인가”를 수치로 보여준다 [40]. 본 연구에서 개인 맞춤형 항생제 감수성 검사표는 임상의와 비슷한 치료 성공률을 보임과 동시에 광범위 항생제 처방을 48-69%나 감소시켜, 일부 광범위 항생제를 선택적 항생제로 대체할 수 있음을 확인했다. 이로서 ML기반의 CDSS가 광범위 항생제 사용을 크게 줄이면서도 치료 성공률을 유지하거나 오히려 높일 수 있었고, 이는 비뇨의학과에서 빈번히 사용되는 Fluoroquinolone과 같은 광범위 항생제에 대한 내성 확산을 늦추는 데 직접적인 기여를 할 수 있을 것이다.
또한, “텔레스튜어드십(telestewardship)”으로 불리는 원격의료(telemedicine) 기반 항생제 관리(antimicrobial stewardship)도 점차 활용되고 있다. 입원 환경에서 원격의료 개입이 항생제 사용량을 줄이고 지침 준수율을 높이는 효과가 일관되게 나타났는데, 연구의 90.9%가 병원 입원 조건에서 항생제 사용량이 5.3%-62.7%까지 유의미하게 감소했다고 보고되었다 [41]. 외래진료를 대상으로 제한한다면 아직은 그 결과가 엇갈려(원격진료가 오히려 과잉 처방 위험을 높인 사례도 보고), 이를 개선하기 위해 플랫폼 설계와 성과 지표·피드백 시스템을 보다 정교하게 만들 필요가 있다. 향후 비뇨의학과 외래 진료와 응급실 진료에서 요검사 결과, 지역 내성률, 환자 과거력등의 데이터를 함께 반영하는 UTI 위험 예측 모델이 유용할 것이다. 이를 활용하면 불필요한 소변 배양검사나 항생제 처방을 줄이고, 꼭 필요한 환자에게만 적절한 항생제를 쓰는 데 도움을 줄 수 있다.
요약하면, AI는 기관·지역 수준의 항생제 관리 전 과정에서 처방을 더 정확하고 덜 광범위하게 만드는데 체계적인 도움을 줄 수 있다. CPOE의 실시간 위험 프롬프트는 입원 초기에 광범위제 DOT을 줄이되 안전성은 유지하게 하고, PAF 우선순위화 모델은 ‘봐야 할 처방’만 골라 스튜어드십 자원을 집중하게 한다. 입원 치료 중에는 AI가 조기 중단 및 경구 전환 시점을 설명 가능한 근거로 제시해 DOT과 광범위 항생제 사용 비율을 낮출 수 있다. 외래 및 지역사회에서는 개인화된 antibiogram과 ML 알고리즘이 퀴놀론 등 광범위제 사용을 줄이면서도 효과적인 치료를 유지할 수 있다. 원격 스튜어드십은 효과가 보고되었지만, 과처방 위험을 피하려면 플랫폼, 성과 지표, 피드백 시스템을 더욱 정교하게 설계해야 한다. 이러한 의료기관 및 지역사회 차원의 항생제 관리에서의 AI의 도입과 확산의 열쇠는 데이터 표준화, 외부검증, 성능 모니터링, 설명가능성, 편향 및 알림 피로 관리이며, 비뇨의학 영역에서는 국내 UTI 진료 현실에 맞는 AI/ML 기반 스튜어드십 알고리즘의 개발과 단계적 도입을 적극적으로 권장해야 한다.
2.4. AI를 이용한 신약·신개념 항균제 설계
전통적인 방법으로 새로운 항균 물질을 개발하는 것은 시간과 비용이 많이 소요되고, 독성 문제와 같은 한계에 직면해있다. 이 때문에 새로운 항균 물질의 발견과 개발 속도가 느려, 급증하는 항생제 내성 문제를 따라잡지 못하고 있는 실정이다. 이처럼 신규 항균제 탐색은 비용이 크고 실패율이 높지만, AI는 후보 물질 발굴부터 최적화, 작용 기전 규명, 내성 및 안전성 위험 예측에 이르는 전 과정을 빠르게 이어주는 도구로 자리매김하고 있다. 대표적으로 딥러닝 스크리닝(deep learning screening)은 수억 개 규모의 화합물 공간에서 전임상 활성 후보를 신속히 추려낸다. MIT-하버드 팀은 1억여 분자를 학습한 모델로 기존 항생제와 구조가 전혀 다른 ‘할리신(halicin)’을 찾아냈고, 동물모델에서 다제내성 A. baumannii 감염을 억제함을 보였다 [42]. 이 연구는 “AI 우선(AI first)” 스크리닝이 새 계열 항균물질을 발굴할 수 있음을 최초로 증명한 사례로, 딥러닝 접근은 기존 항생제와는 다른 작용 기전(mode of action)을 가진 화합물을 찾아내는 데 유용하고, 이는 내성 메커니즘을 우회할 수 있어, 현재의 항생제 내성 문제에 대한 근본적인 해결책을 제공할 수 있을 것이다. 또한 신약 개발에 드는 막대한 시간과 비용을 절감하여 새로운 치료법을 더 빨리 임상에 적용할 수 있게 해줄 것으로 기대된다.
항균 펩타이드(AMP) 설계에서도 AI의 진입이 빠르다. “Molecular de-extinction)”이라는 혁신적인 개념을 도입하여 딥러닝을 통해 멸종된 고대 생명체의 단백질에서 새로운 새로운 항균 펩타이드 후보를 발굴하는 전략이 제시되었다 [43]. 연구자들은 항균 활성을 가진 분자들을 예측하는 새로운 다중 작업 딥러닝 모델인 APEX (Antimicrobial Peptide EXplorer)를 개발하였는데, 이 모델은 기존의 펩타이드 데이터를 학습하여 항균 능력을 예측하는 능력을 갖췄다. APEX 모델을 멸종된 생명체(매머드(woolly mammoth), 거대 나무늘보(giant sloth) 등)의 유전체에서 추출한 1,000만 개 이상의 펩타이드 서열에 적용하여 37,176개의 항균 활성 후보 물질을 식별했으며, 이 중 11,000개 이상은 현재 생명체에서는 발견되지 않는 독특한 분자였다 [그림 2]. 69개의 펩타이드를 실제로 합성하여 실험적으로 항균 활성을 검증했고, 최종적으로 매머드와 거대 나무늘보 같은 고생물에서 유래한 화합물들이 쥐 모델의 감염 치료에 가능성이 있음을 확인하였다. 이들 연구는 대규모 서열공간을 학습해 수천만 개 후보를 신속 선별하고 소수 후보 합성하여 검증하는 워크플로를 확립하고 있다. 임상 적용까지는 제형화, 체내 안정성, 대사 및 배설 등의 과제가 남아 있고, AI 및 ML 기반 접근법의 한계(예: 구조 정보 부족)가 남아 있지만, 향후에는 구조 정보와 다중 목표 최적화 기법을 결합하여 더 우수한 항균 펩타이드를 설계할 수 있을 것으로 전망된다.
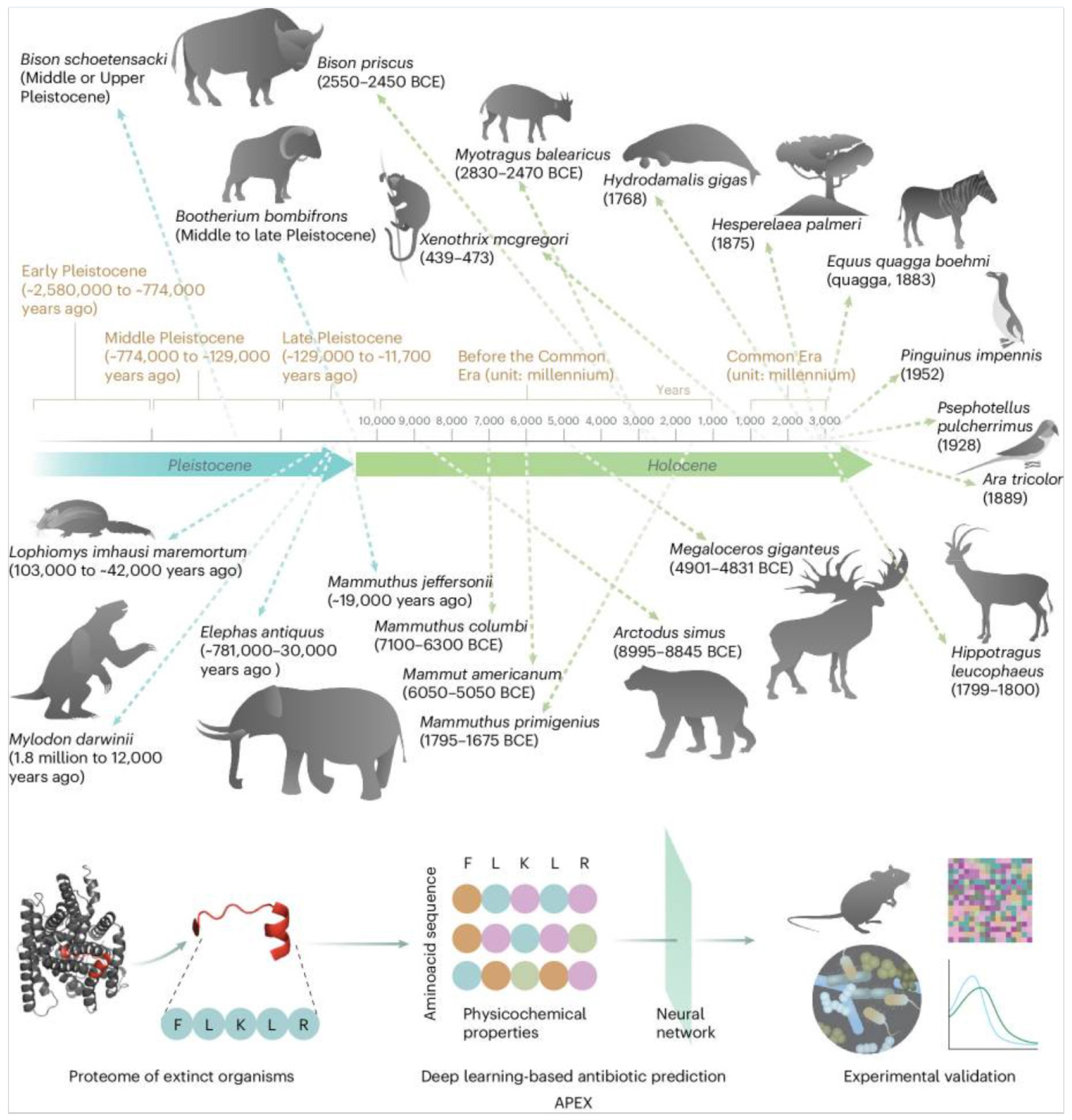
그림 2.
딥러닝을 이용한 ‘분자 복원(molecular de extinction)’으로 고대 단백질체에서 항균 펩타이드 발굴 [43].
멸종 생물의 단백질체에서 8–50개 아미노산 길이의 펩타이드를 추출하고, 딥러닝 모델(APEX)이 항균 활성을 보일 것으로 예측한 펩타이드 후보 물질을 합성, 예측 점수가 높은 후보를 합성해 임상 관련 병원체를 대상으로 시험관 및 동물 감염 모델에서 검증하며, 물리·화학적 특성, 병용 시너지도 함께 평가한다. 그림 상단의 연대표는 각 멸종 종의 추정 멸종 시기를 나타낸다.
그람음성균의 외막은 신약 개발에서 큰 장벽이다. 특히 요로감염의 주요 원인균인 E. coli, Klebsiella, Pseudomonas 등은 외막과 포린 채널 때문에 약물이 세포 안으로 잘 들어가지 못해 개발의 병목이 된다. 이를 해결하기 위해 하버드–일리노이 연구팀은 E. coli 실험 데이터를 기반으로 “잘 축적되는 분자의 물리화학적 특징을 정리한 규칙(eNTRy rules)”을 제시했다. 이어서 특정 포린(OmpF, OmpC 등)을 통과할 수 있는지를 계산 모델로 빠르게 예측하는 방법도 개발되었다. 이런 침투·축적 예측 규칙은 개발 초기 단계에서 약물이 실제로 세균 안에 들어갈 가능성이 있는지 미리 가늠하게 해주어, 임상 개발로 이어지기 어려운 후보를 조기에 걸러내어 연구 자원을 효율적으로 사용할 수 있다 [43]. 신약 개발을 하는 입장에서는 “새로운 약이 요로병원체 안에 실제로 들어갈 수 있는지”를 초기에 판단할 수 있게 된다는 점에서 의미가 크다. 또한, 후보 약물의 작용기전(Mode of Action, MoA) 분류에도 AI가 쓰인다. 예를 들어, 전사체(RNA-seq) 데이터나 세포 형태·세포학적 반응 패턴을 학습시켜, 새로운 후보가 기존 항생제와 같은 계열인지, 아니면 전혀 다른 기전인지를 빠르게 구분할 수 있다. 이렇게 하면 중복 기전 후보는 초기에 배제하고, 새로운 계열 가능성이 있는 약물만 선별해 임상 개발 단계로 빠르게 올릴 수 있다.
현시점에서, AI가 새로운 항균제 후보를 찾고, 항균 펩타이드를 설계하며, 그람음성균 침투 가능성을 예측하고, 작용기전을 분류하는 속도를 크게 앞당긴 것은 분명하다. 그러나 현재까지 AI가 발굴한 대표 후보들(예: halicin, abaucin, 여러 AMP)은 아직 임상시험 단계에 본격적으로 진입한 사례가 많지 않다. 실제 치료제로 이어지려면 흡수·분포·대사·배설(ADME), 독성 평가, 제형화 문제, 그리고 요로 특유의 환경(소변의 pH, 삼투압, 카테터 바이오필름) 같은 현실적인 장벽을 넘어야 한다. 의미 있는 성과를 얻으려면 (1) 진단과 연계해 표적을 좁히고, (2) Pharmacokinetics/Pharmacodynamics (PK/PD) 최적화와 독성 예측을 조기에 진행하며, (3) 다기관 전임상과 초기 임상으로 빠르게 전환하는 과정이 필수적이다.
그럼에도 불구하고, AI는 이미 딥러닝 스크리닝으로 새로운 계열의 항균제를 찾아내고, 생성모델로 수많은 항균 펩타이드 후보를 빠르게 걸러내며, 그람음성균 침투 규칙으로 요로병원체를 더 효과적으로 겨냥하는 변화를 만들어내고 있다. 따라서 임상의가 반드시 알아야 할 ‘실질적 변화’는 이미 시작되었다고 볼 수 있다. 결국, AI는 “새로운 후보를 더 빨리 찾고, 세균 안으로 들어갈 수 있는지 확인하며, 안전성을 일찍 가늠하는 실용적인 도구”라고 할 수있다. 비뇨의학 분야의 감염에서는 이를 활용해 표적을 좁히고, 병용 전략을 설계해 광범위제 의존을 줄이는 핵심 축이 될 수 있을 것이다.
3. 결론
항생제 내성(AMR)은 진단·치료·운영 전 과정을 압박한다. 임상에서는 인공지능(AI)이 신속하고 정확한 진단, 예측 기반 처방, 병원·지역사회 차원의 스튜어드십(AMS), 신규 항균 전략 탐색을 통해 “데이터를 임상 결정으로” 잇는 실용 도구로 자리 잡아 가고 있다. 비뇨의학 영역에서도 신속 AST·MALDI‑TOF+ML로 초기 처방 정확도를 높이고, 개인화 예측·antibiogram으로 광범위제 의존을 줄이며, CPOE 프롬프트·PAF 우선순위화·48–72시간 재평가로 DOT과 2차선 비율을 낮추되 안전성은 유지하게 한다.
대한민국의 강점은 국민건강보험이라는 단일 보험체계, DUR (Drug Utillization Review) 경고, 질병관리청의 다양한 감시체계 등 국가 단위 데이터 인프라와 국산 신속 AST (dRAST) 같은 기술 자산이 이미 존재한다는 점이다. 반면 보완할 점은 분명하다. 첫째, 병원 간 데이터 표준 부재로 전국 단위 통합·확산의 마찰이 크다. 보건 복지부 국제전송기술표준(Fast Healthcare Interoperability Resources, FHIR) 기반 한국형 전송 표준과 공통 코드(진단·약물·감수성·검사)의 표준화를 서둘러야 한다. 둘째, 모델 정확도·보안·수용성에 대한 우려가 남아 있다. 따라서 앞으로 의무기록·유전체·지역 내성·치료결과를 통합한 다변량 학습, 임상 동시 검증, 클라우드 기반 지속 업데이트로 신뢰도를 높여야 한다. 셋째, 현재 감시는 3차병원·중환자 위주여서 1–2차의 경증 UTI 현장을 제대로 반영하지 못하고 있다. 따라서 외래·응급 중심의 실시간 감시/권고 체계를 더욱 보강해야 한다.
향후에는 이러한 기반을 바탕으로, 진료 현장에서 권고·평가·피드백이 하나의 순환 구조로 이어지는 항생제 사용 통합 관리 체계를 구축해야 한다. 예를 들어, 입원 초기에는 저위험군 환자에게 표준 항생제를 우선 제시하고, 48-72시간 후에는 중단이나 경구 전환 여부를 재평가하며, 이후에는 DOT, 2차선 항생제 사용률, CDI 발생률, 재내원율 등 주요 성과 지표를 지속적으로 모니터링하고 피드백하는 방식이다. 이러한 데이터 기반 순환형(closed-loop) AMS 운영 모델은 AI가 실제 임상에 녹아드는 핵심 구조가 될 것이다. 또한 단계적 검증과 확산을 통해 AI 모델의 성능을 향상과 함께 내성률 감소를 투명하게 평가하고, 임상의와 환자 모두가 신뢰할 수 있는 시스템으로 발전시켜야 한다. 궁극적으로 AI의 가치는 화려한 알고리즘이 아니라 환자 곁에서 더 빠르고 정확하며 절제된 항생제 처방을 실현하는 운영 역량에 있다. 이러한 로드맵을 일관되게 실행한다면 ‘AI를 통한 항생제 내성 극복’은 구호를 넘어 현장의 변화로 이어질 것이다.



