1. 서론
불임(난임)이란 임신 가능한 연령의 부부가 피임하지 않고 적어도 1년 이상 정상 성생활을 하였음에도 아이를 출산하지 못하는 상태를 말한다. 그러나 이러한 불임(infertile)은 임신을 못한 경우이지 임신불능(sterile)은 아니다.
결혼한 부부의 15%가 불임이고 이 중 40-60%가 남성쪽에 원인이 있는 것으로 생각된다. 이러한 남성불임은 정액검사의 결과에 따라 크게, 정액검사가 정상인 경우, 정액검사에서 정자는 있으나 질에 이상이 있는 경우(감정자증, 약정자증, 기형정자증 등), 그리고 무정자증으로 대별된다. 이중 무정자증은 병명을 나타내는 용어가 아니라 정액검사에서 정자가 없는 상태를 말하는 것으로 이러한 무정자증도 그 원인에 따라서 치료방향이 달라지며 크게 폐쇄성 무정자증 (obstructive azoospermia; OA)과 비폐쇄성 무정자증(non-obstructive azoospermia; NOA)으로 나눌 수 있다.
실제로 무정자증은 불임남성 5명 중 1명으로, 이 중 31%는 폐쇄에 의해서, 15%는 고환조직은 정상이나 확실한 폐쇄가 없는 경우, 나머지 54%는 고환기능의 부전(不全, testicular failure)인 경우이다. 실제 10년간 제일병원에서 시행한 정액 검사에서도 18.1%에서 무정자증을 보이고 있다.
폐쇄성 무정자증의 치료에 있어서, 선천성 정관형성 부전증(congenital bilateral absence of vas deferens; CBAVD)이나 수술적 교정이 불가능한 폐쇄성무정자증(부고환 전체의 폐색, 부고환 형성부전 정자증)에서 부고환이나 고환내 정자를 이용한 난자세포질내정자주입술(Intracytoplasmic sperm injection; ICSI)을 실시하면 임신에 도달할 수 있다.
그러나, 이러한 ICSI를 이용한 경우는 주로 고환기능이 정상인 폐쇄성무정자증 환자에서 시도되어 왔으며, 고환기능의 부전으로 인한 비폐쇄성 무정자증환자와 클라인펠터증후군에서는 비배우자 인공수정(Artificial insemination of donor, AID)이나 입양하는 것이 치료의 전부였으나, 미세수술적다중적고환조직정자채취술(m-TESE; microsurgical Testicular Sperm Extraction)을 통하여 임신에 성공하고 있다.
2. 본론
2.1. 무정자증의 진단
무정자증 환자에서 폐쇄성(OA)인지 비폐쇄성(NOA)인지 감별하여 수술적 교정이 가능한지를미리 아는 것이 중요하며, 그 다음 단계로 고환내 정자채취의 가능성에 대한 평가, 무정자증의 유전적 원인에 대한 진단, 보조생식술과 적절한 유전적 상담을 위해 다음과 같은 검사과정을 시행한다. 이러한 검사를 시행함에 있어 염두에 두어야 할 것은 비침습적(noninvasive)이고 경제적(cost-effective)이어야 한다.
2.1.1. History
어릴 때 고환염이나 mumps orchitis의 병력, 정관의 손상을 유발할 수 있는 음낭수종이나 탈장수술의 과거력 및 나중에 역행성 사정을 초래할 수 있는 방광 경부의 Y-V plasty와 후복막 임파절제술(RPLND)의 과거력을 알아야 한다. 또 정자생성의 장애를 초래할 수 있는 약물의 복용 유무도 알아야 한다 [표 1].
표 1.
남성불임에 관련된 과거력
2.1.2. Physical examination
이학적 검사의 이상은 내분비 질환이나 염색체이상을 시사해준다. 특히 고환과 음낭의 자세한 진찰이 제일 중요한다. Orchidometer를 이용한 고환의 크기는 생식기능의 이상유무를 미리 예측할 수 있는 가장 좋은 지표이다. 한국인의 고환크기는 평균 19 ± 5 ml로 이보다 작을 때는 생식기능의 이상이 있음을 시사해 준다. 정관의 유무를 반드시 확인해야 되겠다. 정관의 유무로 선천성 정관형성 부전증(congenital bilateral absence of vas deferens; CBAVD)의 진단이 가능하다.
2.1.3. Semen analysis
정액검사에서 무정자증이 나오면 원심분리를 하여 더 세밀한 정액검사를 하여야 한다. Fructose를 검사하여 사정낭의 폐쇄 유무를 알고 역행성 사정에 의한 무정자증도 감별해야 한다.
2.1.4. Endocrine evaluation
남성불임의 내분비적 원인은 시상하부-뇌하수체-고환의 축에 대한 평가에 의해 진단되며, 주로 FSH, LH, testosterone, prolactin을 측정한다. 최근에는prolactin 검사의 무정자증에서 임상적 효용이 떨어져 시행하지 않는 편이다. 이 중 FSH가 무정자증에서 특히 중요한 의미를 갖는다. FSH는 Sertoli cell을 자극하여 정자의 형성과 성숙을 촉진시키는데 고환기능부전으로 정자형성장애가 있을 때 FSH는 증가되므로 무정자증에서 고환 내 정자형성의 가장 중요한 지표가 된다. 일반적으로 고환기능이 이상이 없는 페쇄성무정자증의 경우 FSH는 정상 범위이며 정자형성에 장애가 있는 경우에 FSH는 상승하나, 고환조직 정자채취술(Testicular sperm extraction; TESE) 시행 시 정자 채취가능성의 절대적인 기준은 아니다.
2.1.5. Testicular biopsy
무정자증의 경우, 이전에는 고환의 상태를 알기 위하여 고환조직검사를 시행하였다. 그러나 최근에는 호르몬 검사와 고환 진찰에서 비 폐쇄성 무정자증이 확실하다면 굳이 고환 조직 검사를 할 필요는 없다. 또한 난자세포질내 정자직접주입법(intracytoplasmic sperm injection; ICSI)의 도입으로 고환조직검사의 진단적 가치와 함께 TESE라는 불임남성의 치료목적으로도 시행되기 시작하였다 [표 2].
표 2.
고환조직검사의 적응증
| 1. Diagnostic Distinguishing between obstruction and testicular failure |
| 2. Diagnostic Identification of mature sperm for ICSI |
| 3. Therapeutic Harvesting of sperm for ICSI |
2.1.6. Genetic study
남성에서 불임을 유발하는 유전적인 원인으로는 염색체 수준의 이상과 단일 유전자 수준의 이상으로 구분할 수 있다. 염색체 수준의 이상으로는 Klinefelter’s syndrome (47, XXY), translocation, XYY등이 있는데, 여러 문헌의 보고에 따르면 염색체이상의 빈도는, 무정자증 환자에서 13.7%, 감정자증에서 약 4.6%. 정상인에서 0.38%로 무정자증에서 높음을 알 수 있다. 단일 유전자수준의 이상은 최근 분자생물학과 유전학의 발달로 이러한 유전자들의 돌연변이가 분석되고 또 새로운 유전자들의 돌연변이가 관찰되고 있다. 대표적으로 Y염색체의 미세결실과 CBAVD를 유발하는 cystic fibrosis transmembrane regulator (CFTR) 유전자 등이 있다. 무정자증의 10-15%에서 Y염색체의 미세결실이 보고되며 CBAVD의 50-82%에서 1개 이상의 CFTR gene의 돌연변이가 보고되나 우리나라에서는 아직 확실한 빈도가 보고되고 있지 않다 [표 3].
표 3.
남성불임과 관련된 유전적 질환
ICSI의 출현으로 남성 불임치료에 획기적인 혁명이 왔지만 동시에 이러한 의문점을 제시할 수 있다. 문제가 있는 정세관에서 추출된 유전학적으로 문제가 의심이 되는 정자나 원형정자(spermatid)의 사용이 과연 문제는 없는지?, 남자 후손 출생 시 불임이라는 똑같은 문제가 유발되지는 않을지? 등이 의문시되고 있다. 정자생성과정은 단순히 Y염색체 한 부위의 조절을 받기보다는 복잡하고도 복합적인 과정에 의해 영향을 받는데, 최근 Y염색체 말고도 상염색체에서도 이에 관여하는 부위가 있는 것으로 생각된다. 실제 위의 이런 염색체 이상이 ICSI를 시행할 경우 후손에게 전달될 가능성이 있다고 할 때 부부가 시술 전 이 사실을 충분히 이해하는 것이 중요하다. 그 이유는 그들이 이 사실을 충분히 이해한 뒤에 이런 시술을 원하지 않을 수도 있기 때문이다. 즉, 자세하고도 충분한 설명과 임신이후에도 세심한 관찰이 필요한 것이다. 염색체이상이나 유전자 이상에 의한 남성 불임 환자의 경우 ICSI를 할 경우 이러한 염색체이상이나 유전자 이상이 자손에게 유전될 가능성이 있으므로 무정자증에서 유전적 원인에 대한 진단은 유전 상담을 위하여 반드시 필요하다.
2.2. 무정자증의 치료
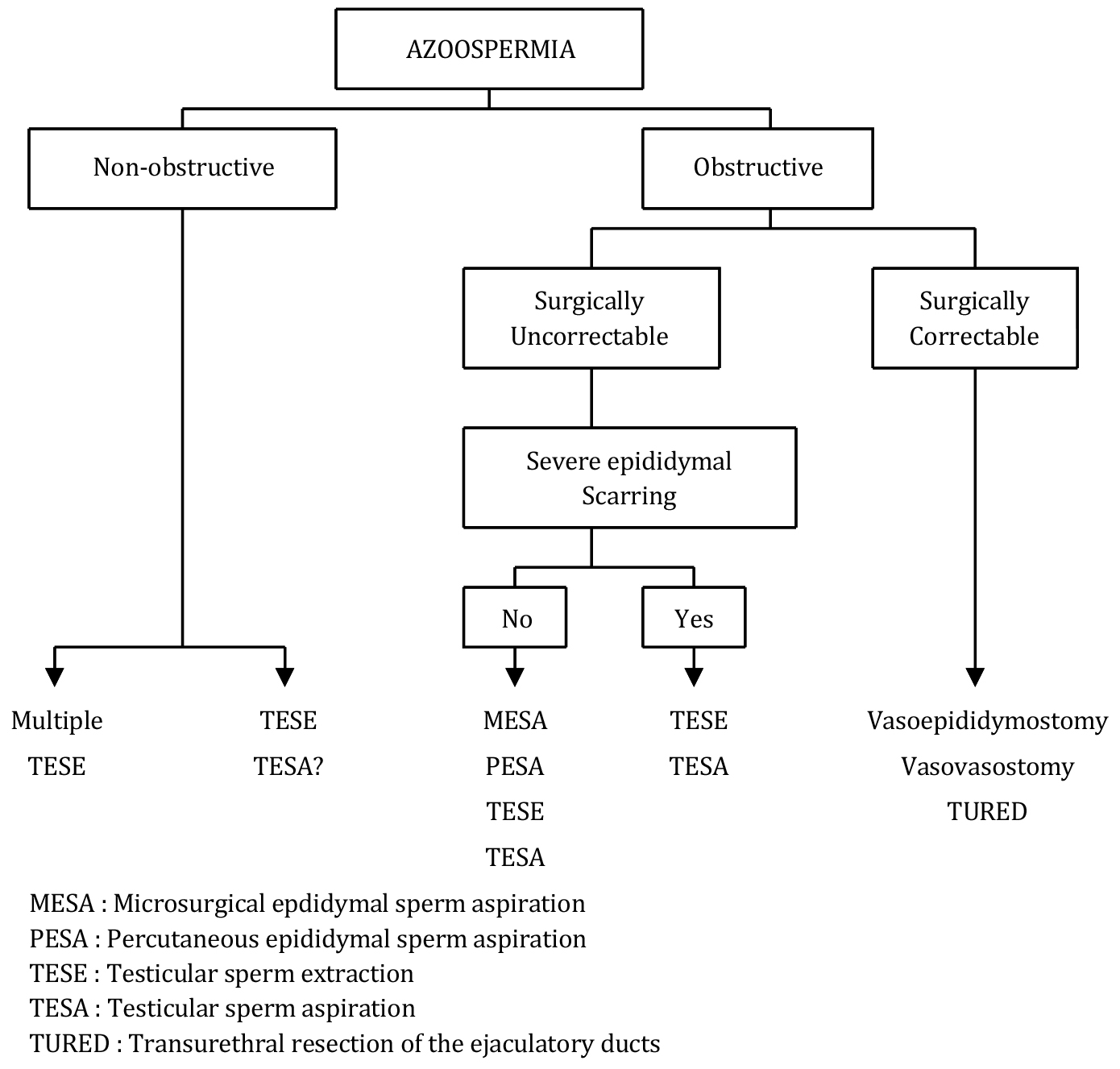
2.2.1. Decision-making for sperm retrieval [그림 1]
무정자증 환자에서 ICSI를 하기위한 정자 채취 시, 정자채취의 방법과 장소 결정에 가장 중요한 것은 환자가 “폐쇄성(OA)인지 비폐쇄성(NOA) 무정자증인지” 이다. 만약 비폐쇄성(NOA) 무정자증이라면 그 장소는 고환이 되겠지만, 폐쇄성(OA) 무정자증이라면 폐쇄의 근위부 부위부터 정자채취를 하게 된다.
비폐쇄성 무정자증의 경우 FSH나 고환 크기의 상관 관계없이 고환조직에 상관하여 정자가 발견된다 [표 4, 5]. 최근에는 클라인펠터 증후군에서도 TESE에 성공하여 건강한 남아가 태어났고, 정계정맥류가 있는 비폐성 무정자증의 경우 수술 후 유정자로 바뀐 사례가 보고되고 있다.
표 4.
성선자극호르몬 수치에 따른 정자 발견 성공률
3. 결론
1978년 체외수정으로 첫 아기 루이스 브라운양이 태어난 지 24년이 지났다. 그리고 이후 생식의학분야에서도 많은 발전이 있었다. 특히 난관폐쇄라는 여성불임 해결을 위한 일반적인 체외수정과 수정율과 임신성공율을 높이려고 시도한 ICSI는 첫 의도와는 달리 남성불임치료에서 가장 많은 변화를 가져왔다.
MESA, TESE의 도입으로 이전에 치료되지 않는 불임 환자 부부에게 새로운 희망을 주었다. MESA-ICSI는 미세수술(부고환 정관 문합술, 정관 정관 문합술등)이 실패한 불임 환자인 경우에도 해결점을 제시하였다. TESE-ICSI의 경우 이제 고환 조직을 냉동 보관하여 사용하는 단계에 이르렀다. 미세조작술의 발전으로 비폐쇄성 무정자증에서도 임신에 성공하고, 정자 전 단계인 원형정자(round spermatid)나 제2정모세포(secondary spermatocyte)에서도 이론적으로 ICSI가 가능하게 되었다.
특별히 여성의 문제나 수술적 교정이 불가능한 경우 MESA-ICSI나 TESE-ICSI가 치료의 첫 선택이 되겠으나 정계정맥류가 있거나 정관정관 문합술이나 미세 수술적교정이 가능한 경우는 수술적 교정이 치료의 첫 선택임은 주지의 사실이다.
그러나 무엇보다도 중요한 의문점 몇 가지가 다음과 같이 제기될 수 있다.
첫째, 왜 이러한 남성불임이 생기는 것일까? 물론 이런 환자들의 대다수가 새로운 신기술로 해결될 수 있겠지만 남성불임의 진단과 그 원인을 해결하는 중간과정이 생략된 채 치료만 있어서는 안 될 것이다.
둘째, 실제로 계속하여 ICSI를 이용한 체외수정을 할 때 임신에 실패한 경우 또 다른 이유는 없는 것일까?
셋째, 정액의 질적인 문제가 있는 경우 이의 치료를 통한 임신방법은 없을까? 그리고 무엇이 이런 사람에게 가장 성공적이고 효과적인 방법일까?
넷째, 문제가 있는 정자를 이용해서 아기가 태어날 때 과연 유전적인 문제는 없을까?
이러한 의문점들을 해결해 나가는 것 역시 남성불임을 극복하는데 있어서 중요한 과제이며, 계속적인 연구가 이루어져야 할 것이다.