1. 서론
2. 본론
2.1. 생식세포 돌연변이(germline mutation), 체세포 돌연변이(somatic mutation)에 의한 전립선암 발생 모델
2.2. 진단
2.3. 누구를 대상으로 유전자검사를 시행할 것인가?
2.4. 유전자검사 결과 보고
3. 결론
1. 서론
전편에서 인간 삶에 있어서 유전자의 역할에 대해 간략하게 알아보았다. 본편에서는 발표된 내용을 토대로 주로 유전자 분석에 관해 이야기하고자 한다.
일반적으로 유전자검사는 크게 2가지 목적으로 시행되고 있다.
1.체세포 돌연변이로 발생한 비유전성 암 환자의 예후 판정하거나, 일반적인 항암치료 후 재발하는 종양의 유전자 변이를 확인하고 변이 유전자가 관여하는 분자생물학적 경로를 역 추정하여 그 경로를 차단할 약물선택에 사용한다. 우리나라에서 일부 악성종양을 대상으로 약물선택을 위한 유전자검사가 시행되고 있으며, 검사비 또한 의료보험으로 지원되고 있다.
2.전립선암과 같은 일부 악성종양 발생은 생식세포의 유전자 변이로 발생하며 종양 발생은 가족 간에 높은 연관성을 보인다. 이러한 생식세포의 돌연변이에 의한 전립선암 발생은 환경적인 요인에 의해서도 영향을 받을 수 있는데, 유전자검사를 통해 확인한 생식세포의 돌연변이를 가진 환자는 종양 발생 가능성이 선천적으로 높지만, 종양 발생에 관여하는 환경을 조절함으로써 종양을 억제하거나, 또는 주의 깊게 시행된 암 검사를 통해 조기에 암을 발견하고 완치할 수 있다.
우리가 유전에 관해 관심이 없어도 의학은 이미 이 방향으로 발전하고 있고 미래에도 그러할 것이다. 따라서 우리가 하지 않으면 미래에는 한의학이나 생물학 등의 유사의학에서 그 주도권을 가지고 갈 것이다. 환자를 보는 임상의가 이해하기에는 어려운 면이 있겠지만, 미래에 대한 투자라 생각하고 관심을 가졌으면 한다.
2. 본론
2.1. 생식세포 돌연변이(germline mutation), 체세포 돌연변이(somatic mutation)에 의한 전립선암 발생 모델
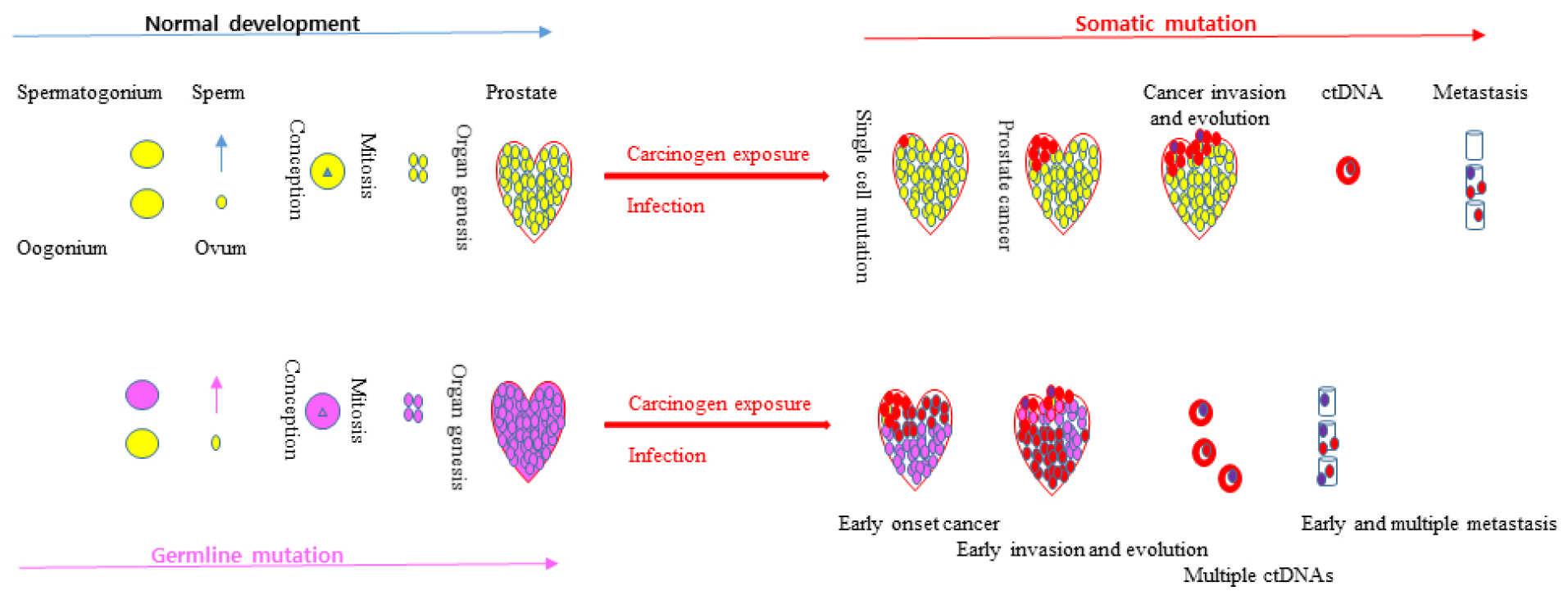
그림 1.
생식세포 돌연변이와 체세포 돌연변이에 의한 종양 발생 차이. 생식세포 안에 존재하는 핵산 변이 혹은 minor allele에 따른 유전정보를 통해 부모에서 발생하는 질병이 자식에게도 전달된다. 따라서 자식은 태어나면서 질병 발생 가능성을 가지고 태어나 일반인과 비교하면 암이나 질병 발생에 선천적으로 취약하고, 암이 발생하면 체세포 돌연변이에 따른 종양과 비교해 어린 나이에 다발성으로, 그리고 빠른 전이를 보인다. 그러나 일반인에서 발생하는 체세포 돌연변이에 의한 암 발생은 생식세포 돌연변이와 비교해 오랜 시간에 거처 발생하고 유전되지 않는 특징을 가진다.
2.1.1. 생식세포 돌연변이
전편에서 언급한 것과 같이 인체를 구성하는 세포는 감수분열을 통해 부모와 다른 새로운 유전자 변이가 발생하거나, 혹은 부모의 변이된 유전자를 물려받은 정자와 난자가 결합하는 수정과정을 통해 하나의 모세포를 만들고, 모세포의 유사분열을 통해 수많은 세포로 증폭하여 생명 유지에 필요한 여러 장기가 만들어진다. 즉, 각 장기의 기능은 달라도 구성하는 모든 세포의 핵산은 원칙적으로 모세포와 같다, 따라서 생식세포 돌연변이에 따른 유전성 질환을 확인하려면 단순하게 구강이나 혈액에서 핵산을 채취해 변이를 검사할 수 있다.
생식세포 돌연변이에 의한 암은 다음과 같은 임상적인 특징을 가진다. ① 암 발생 가족력이 있다. ② 체세포 돌연변이에 의해 발생하는 암에 비교해 악성종양은 젊은 나이에 발생하는 경향을 보이고, ③ 암이 한 장기나 혹은 여러 장기에 다발성으로 발생하고 ④ 비교적 드문 악성종양이 발견되기도 한다.
분자생물학적으로 보면, 암 발생의 원인이 되는 생식세포의 돌연변이는 선천적이거나 수정전 단계인 1차 감수분열 때 시작되며, 이후 살아가면서 축적되는 빈번한 체세포 돌연변이의 발생, 혹은 나이가 듦에 따라 암 억제 면역 약화 등으로 일반인에게서 관찰되는 체세포 돌연변이 보다 일찍 악성 암이 발생한다. 생식세포의 변이가 있어도 바로 암이 발생하는 것이 아니라 출생 후 지속적인 유발요인에 의한 자극이 있어야 한다. 즉, 암 발생은 일정한 시간이 필요한 암 발생에 필요한 단계를 거쳐 발생한다. 만일 이러한 발생단계들을 규명할 수 있고 각 단계의 진행을 억제할 수 있는 물질(chemoprevention: aspirin의 colon-rectal cancer 예방) 등이 개발된다면 악성화 과정을 되돌리거나 그 진행을 억제할 수 있다 [그림 2].
따라서 병력에서 생식세포 돌연변이에 의한 악성종양 발생이 의심되면 ① 환자와 혈연관계에 있는 사람들을 대상으로 조기에 유전자검사를 시행하고, 유전적인 요인이 발견된다면 종양 발생에 관계하는 환경을 일반인보다 더 엄격하게 통제하거나, 종양 발생을 억제하는 환경을 조기에 도입하여 특정 암 발생을 억제할 수도 있다. 또한, ② 전립선암의 경우 유전적 요인과 환경적 요인 모두 암 발생에 관여한다고 알려져 있고, 암 발생은 Prostatic intraepithelial neoplasia (PIN) 등의 전암 단계를 거쳐 전립선암이 발생한다. 붉은 육류 등의 특정 음식이 전암 단계에서 전립선암으로 진행을 촉진한다. 따라서, 암 진행이나 발생에 관여하는 식단을 엄격하게 조절하여 PIN에서 악성종양으로 진행되는 것을 억제할 수 있다는 연구도 많다. 즉, 전립선암의 유전적 소인이 있는 환자를 조기에 발굴하여 환경적 요인을 잘 조절하여 전립선암으로 진행을 늦추거나 억제할 수 있고, 유전적 소인이 있는 환자들을 대상으로 PSA screening 검사 등을 조기에 도입하거나 좀 더 엄격한 관리를 통해 전립선암을 초기에 진단하고 치료해 완치에 이를 수도 있다.
2.1.2. 체세포 돌연변이
수정과정과 유사분열을 통해 정상적으로 만들어진 장기를 구성하는 세포에 돌연변이 유발요인들이 지속적이고 강하게 노출된 후 체세포 돌연변이가 발생하여 악성종양이 발생하게 된다. 체세포 돌연변이를 확인하기 위해서는 정상 세포와 악성종양 조직 사이에 유전자 비교가 필수적이다. 따라서 악성종양의 유전자를 얻기 위해 종양의 수술적 처치나 조직검사 등이 필수적으로 동반되어야 한다.
체세포 돌연변이에 의한 암 발생의 특징은 생식세포 변이와 비교해 뚜렷한 암 발생 가족력이 없고, 비교적 늦은 나이에 발생하며, 단일 장기에 단일 종물로 발견된다. 종양 환자의 전체를 보면 체세포 돌연변이에 따른 종양이 대부분을 차지하고 생식세포 돌연변이에 따른 악성종양 발생은 소수에서 발견된다. 분자생물학적으로 체세포 돌연변이는 암 발생의 원인이 후천적으로 제공되었음을 의미하며, 살아가면서 축적되는 빈번한 체세포 돌연변이 발생, 혹은 나이가 듦에 따라 암 억제 면역 약화 등으로 발생하며, 종양은 성장함에 따라 혹은 항암제와 같은 약물치료 과정 중에 다양한 유전자 변이가 새롭게 만들어지며 종양의 생존을 도모하고 있다.
2.2. 진단
2.2.1. 유전자 변이에 따른 질병 진단과 한계 [그림 3]
유전자검사를 통해 질병을 예측할 수 있다고 하지만, 2가지 경우를 생각해야 한다.
① 단일 유전자 변이만 관찰하여도 질병 진단 정확도가 100%에 이를 정도로 높지만(높은 penetration), 임상적으로 그와 같은 환자를 만날 확률은 매우 낮은 질병군이 있다(낮은 allele 빈도). 예를 들면, 멘델 유전법칙에 따라 유전되는 질병은 단일 유전자 변이로 발생 되는 경우가 많은데, 임상 증상이나 증후에 따라 Sanger sequencing과 같은 단일 유전자검사를 시행해 쉽게 진단할 수 있지만, 멘델 법칙에 따른 질환은 매우 드물다.
② 질병 진단에 단일 유전자검사의 정확도가 매우 낮아 수많은 유전자 변이를 조합해 확률적으로 질병을 예측할 수 있는 질환을 생각할 수 있는데, 암이나 당뇨, 고혈압, 악성종양 등 대부분 질병이 이와 같은 양상을 보인다. 따라서 대부분의 질병 예측은 단일 유전자 변이보다는 유전체 전반에 거친 유전자 변이를 조사함으로써 추정할 수 있다. Human genome project (HGP) 등의 연구를 통해 인간유전체 전장(whole genome sequences)이 판독, 발표되어 모든 유전자에 대한 변이의 기준이 설정되었으며, 이어지는 Next generation sequencing (NGS) 기법을 통해 저렴하고 신속하게 각 개인의 유전체 전장을 확인할 수 있다.
2.2.2. 멘델 법칙에 따르지 않는 생식세포 돌연변이나 체세포 돌연변이로 발생하는 질환 유전자(biomarker) 발굴: Genome-wide association study (GWA study, or GWAS)
전편에 기술된 것과 같이 인체 내 유전정보는 자연 변이, 인종 간의 차이, 인류의 이동 등에 따라 수많은 유전자 변이가 관찰될 수 있는데, 어떤 변이된 유전자(체세포 돌연변이)나 생식세포 돌연변이에서 관찰되는 소수 유전자형(minor allele)이 질병 발생에 관여하는지를 확인하기 위해서는 생식세포 돌연변이의 경우 질병 발생군과 비 발생군의 대조연구가 필요하고, 체세포 돌연변이의 경우 환자의 암조직과 정상조직을 대상으로 유전자 비교연구가 필요하다.
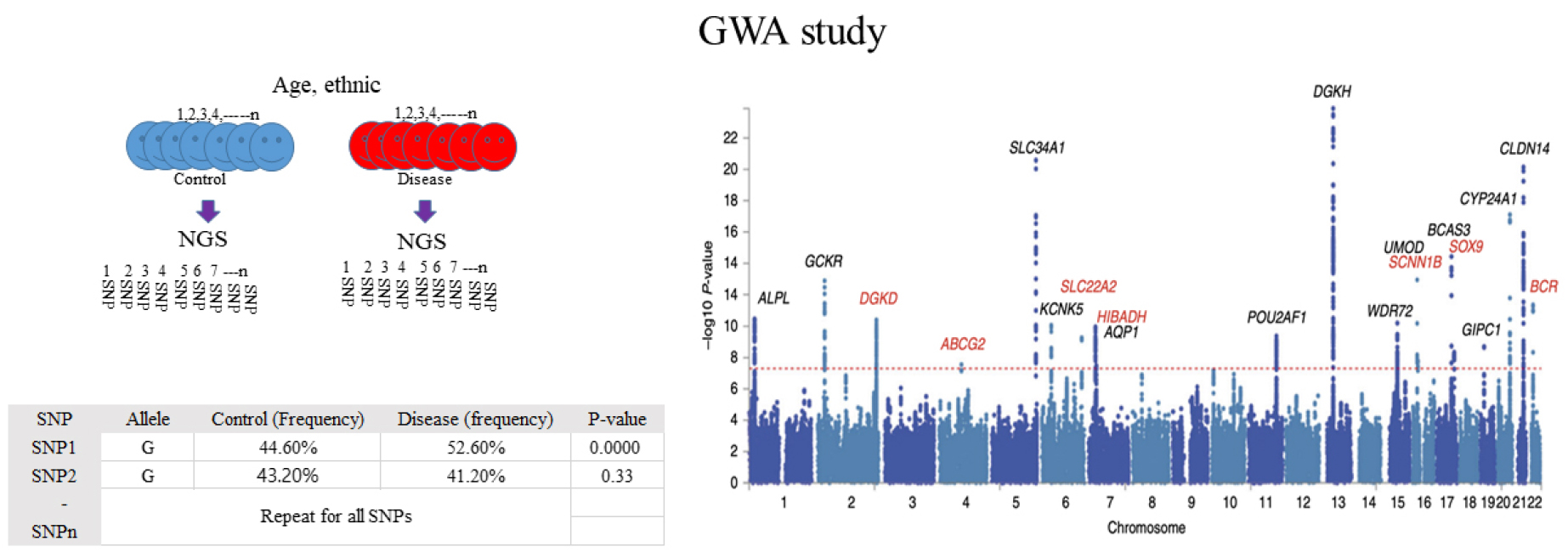
생식세포 변이의 경우 임상적으로 세분된 자료를 기반으로 질병 유/무를 제외하고는 유사한 조건(나이나 인종 등)을 가진 사람을 대상으로 질병군과 대조군으로 나누고, 이 두 군을 대상으로 NGS를 시행해 유전자를 비교 분석하는 방법이 GWA study 이름으로 개발되었다.
전립선암의 경우 많은 검체를 대상으로 NGS 검사를 시행하면 좋겠지만, 시간이나 연구비 제약 등으로 비슷한 나이 분포(전립선암의 경우 노령층에 암 발생률이 높아 대조군/대상군 사이에 나이 차이가 없어야 한다)와 같은 인종(전립선암의 경우 인종에 따라 암 발생률이 차이가 있어 동일 인종에 관해 연구하는 것이 좋다)을 대상으로 GWA 연구를 시행하고 있다. 따라서 다른 나라 결과 혹은 다른 인종의 결과는 우리 한민족의 결과와 일치하지 않아 우리 국민의 특이한 유전자 변이나 질병 마커를 찾기 위해서는 우리 국민을 대상으로 한 GWA 연구가 필요하다.
GWA 연구의 예시로 신장결석 발생에 관여하는 유전자를 확인해보자. 먼저 신장결석이 있는 군과 없는 군의 환자를 모집하고 환자의 핵산을 뽑고, 이를 대상으로 NGS를 시행한다. 나온 결과는 수 많은 A/T/G/C로 즉 4개의 nucleotide로 표기되지만, A/T, G/C가 상보 결합함을 고려한다면 AT--->A로, GC--->G로 표기하고, 이를 표준염기서열(HGP)과 비교해 SNP1 (G type: control 44.6%, disease 52.6%가 나왔다면) 양 군의 차이를 카이제곱 검정을 통해 통계학적 차이를 구한다, 이를 SNP 2, 3, 4, 5,---,N 반복한다. 통계학적 결과를 맨해튼 plot으로 표시한다(https://en.wikipedia. org/wiki/Genome-wide_association_study 참조).
2.2.3. 어떤 유전자 변이가 질병 발생이나 진행에 중요한 역할을 하는가?
NGS를 통한 변이 연구를 진행해보면 연구의 교란변수(나이, 인종, 질병의 다양성) 등에 따라 다양한 결과가 나오고, 통계학적으로는 다중비교분석(multiple comparison)에 의해 p-value가 낮게 나와 일견 의미 있는 결과로 보이지만, 반드시 임상적으로 중요한 의미로 해석되지 않을 수도 있다. 따라서 변이결과와 다양한 임상적인 상관관계를 통해 그 의미를 재분석하는 것이 필요하다.
① 생식세포 돌연변이의 임상적 의미 등급 분류법
생식세포 돌연변이에 대한 임상적인 등급은 잘 알려지지 않았다. NIH (National Institutes of Health:NCBI)에 보관된 dbSNP 자료를 보면, “benign, conflicting interpretations of pathogenicity, likely benign, likely pathogenic, pathogenic, pathogenic likely pathogenic”으로 분류하고 있다.
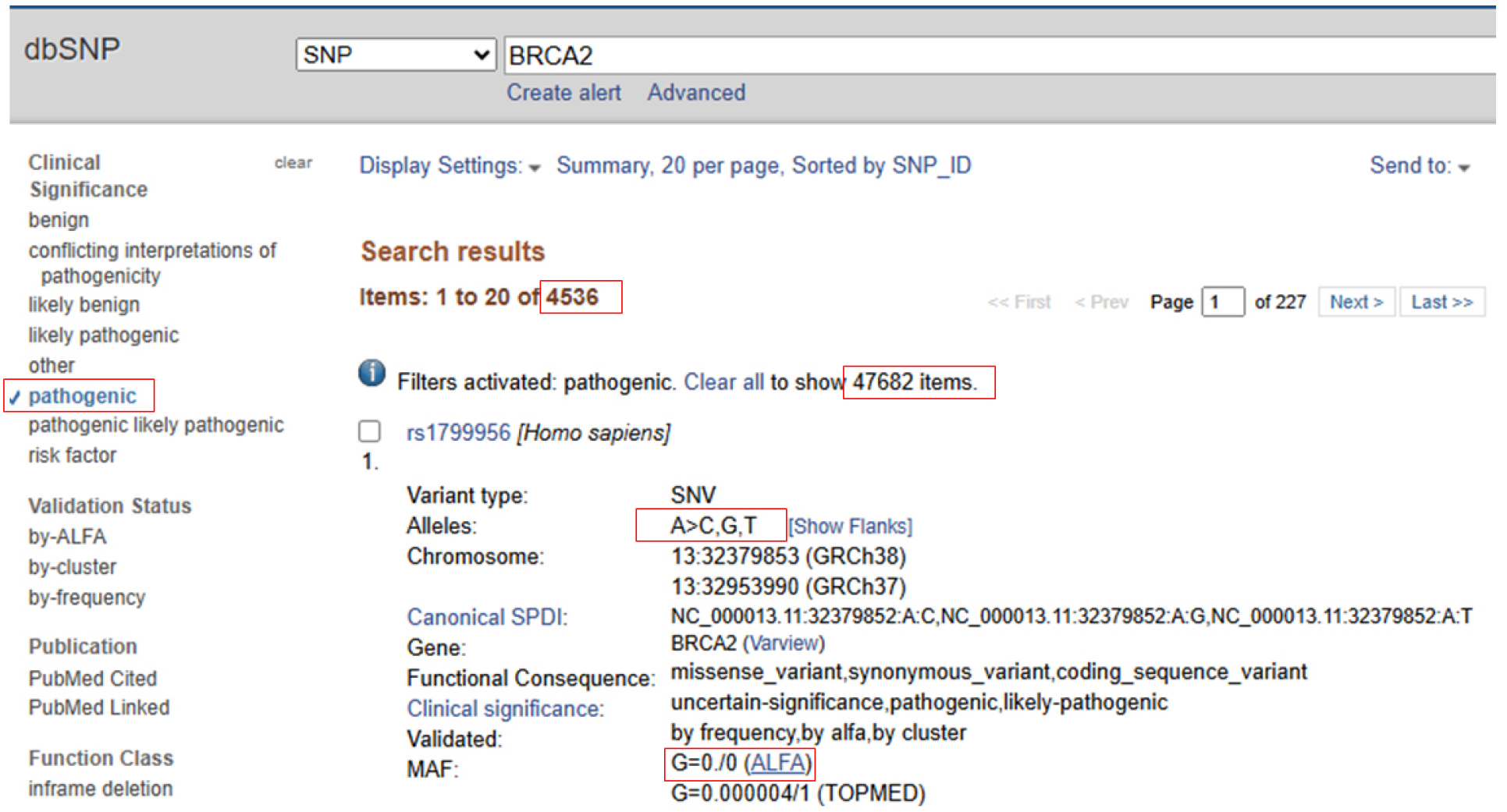
생식세포 돌연변이의 예로 BRCA2 유전자에 대해 알아보자. 먼저 NCBI site에 있는 SNP site에 접속해 BRCA2를 입력하면 아래와 같은 그림 [그림 5]이 나온다. BRCA2 유전자에서 관찰되는 유전자 변이는 47,682개며 이중 pathogenic SNP는 4536개다. 4536개 중 1례인 rs1799956의 경우를 보자. 일반인을 대상으로 시행한 유전자형 분포를 보면 거의 100% (99.9996%)에서 A allele가 관찰되고 단지 0.0004%의 극소수에서만 G allele가 관찰된다(ALFA study, TOPMED study). 이처럼 생식세포 돌연변이가 발생할 가능성이 거의 없는 유전자의 변이는 악성종양 발생에 관여할 가능성이 클 수가 있다.
② 체세포 돌연변이의 분류법
생식세포 돌연변이와 비교해 체세포 돌연변이는 Association of Molecular Pathology (AMP), American Society of Clinical Oncology (ASCO), 그리고 College of American Pathologists (CAP) 등의 공신력 있는 기관에서 체세포 돌연변이를 임상자료 등과 비교 분석해 신뢰도를 가지고 돌연변이를 분류하였다.
표 1.
AMP/ASCO/CAP에서 제시한 암 조직의 유전자 체세포 돌연변이 분류법
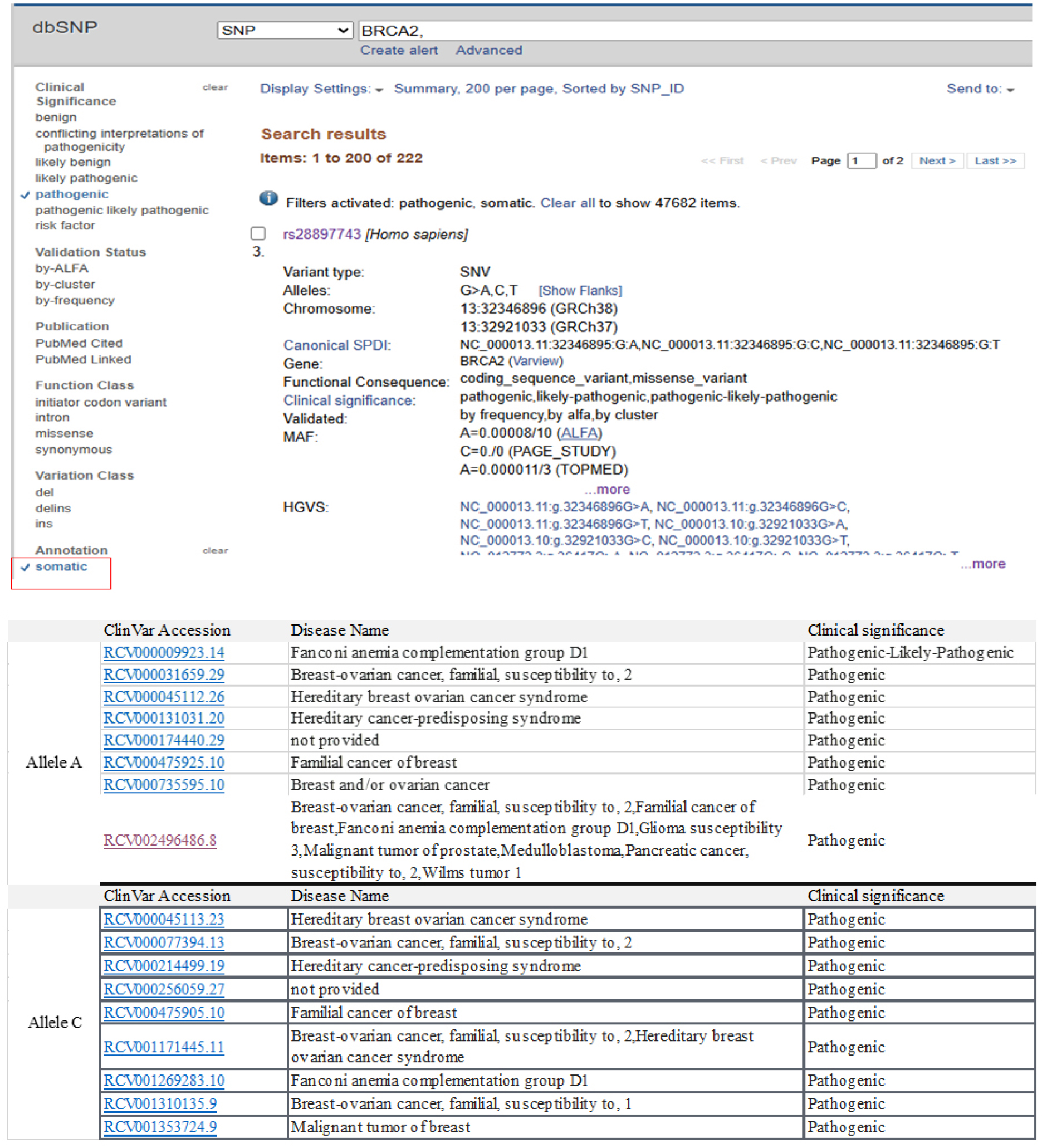
체세포 돌연변이의 경우 정상조직과 비교해 악성종양 조직에서 발견되는 수많은 유전자 변이 중에 Tier1, Tier2 변이만이 임상적 의미가 있다. 참고로 NCBI site에 somatic으로 찾으면 222개의 SNP를 찾을 수 있는데 rs28897743의 경우로 예를 들어보면, 유전적으로 대부분 일반인은 G allele를 가지지만, 극소수에서만 A/C allele를 가짐을 알 수 있다 [그림 6]. 정상적으로는 잘 관찰되지 않는 rare allele가 암 조직에서는 빈발하게 관찰된다. dbSNP site에서 유전자 변이와 관련되어 발표된 임상 논문은 현재까지 18개가 있어 찾아볼 수 있으며, 이 유전자의 변이와 질병 발생은 다음과 같다.
자세하게 보면 동일 유전자 변이가 체세포 돌연변이와 생식세포 돌연변이 모두에 관여할 수 있다. 예를 들면 BRCA 유전자의 생식세포 돌연변이는 가족력이 있는 유방암 발생에 관여한다는 것이 잘 알려졌지만, 같은 변이가 전립선암의 체세포 돌연변이에도 발견되어 항암제 선택에 이용되기도 한다. 따라서 특정 유전자가 악성종양 발생에 관여하는 기전중 멘델 법칙에 따른 유전병을 제외하고는 생식세포 변이 혹은 체세포 변이 중 하나의 유전자 변이만으로 설명하는 것은 한계가 있다.
2.3. 누구를 대상으로 유전자검사를 시행할 것인가?
비뇨기초의학연구회에서 출간한 가이드에 다음과 같이 기록되어 있다.
1) 체세포 돌연변이 검사
기존 치료에 재발하는 악성종양의 치료 방침 결정에 사용될 수 있다. 예를 들어 전이성 전립선암은 anti-androgen으로 1차 치료하지만, 일정한 시간이 지나면 암은 다시 성장하고, 2차 치료로 docetaxel 등과 같은 기존 항암제를 사용해 치료하지만, 악성종양은 일시적인 반응을 보이다가 궁극적으로 재발한다.
예를 들면, 전이성 전립선암(metastatic castration-resistant PC: mCRPC) 환자의 전립선암 조직에서 BRCA 유전자의 변이가 있는 경우, PARP (poly ADP ribose polymerase )억제제인 olaparib나 rucaparib 등이 생존율 개선 효과가 관찰되어(pivotal PROfound and TRITON2 clinical trials) 2020년부터 미국 FDA에서 사용 승인을 하였다. 그 외 여러 유전자 돌연변이에 따른 항암제 치료가 안내서에 잘 수록되어 있다. 때에 따라서는 체세포 돌연변이가 있어 종양이 발생한 때도 생식세포 돌연변이를 조사해 예후 등을 판정하는 데 이용된다.
2) 생식세포 돌연변이 검사
앞의 [그림 5], [그림 6]에서도 제시된 것과 같이 일반인이 특정 유전자에 대해 생식세포 돌연변이를 가지는 것은 매우 드물다. 따라서 모든 건강검진 환자를 대상으로 시행되는 것보다는 질병 가능성이 큰 사람을 선별해 검사함이 옳다. 즉 본인에게 발생한 암이 유전으로 발생하였다는 강력한 증거가 있다면 생식세포 돌연변이 검사할 수 있다. 또한, 혈연관계에 있는 사람에게 유전자검사를 권유할 수도 있다.
예를 들면 전립선암의 선별 유전자검사의 추천 대상 환자는 다음과 같다.
•본인 전립선암 외 다른 장기의 원발암 진단의 과거력(multiple primary cancers)
•부모, 형제, 자녀에서 60세 이전 진단된 전립선암 또는 전립선암으로 인한 사망
•부모, 형제, 자녀, 조부모, 손자녀와 사촌 내 혈족 중 50세 이전 진단된 유방암, 대장암 또는 자궁내막암, 또는(진단 연령과 관계없이) 난소암,(외분비) 췌장암 또는 고위험/전이성 전립선암 경우.
•부모, 형제, 자녀, 조부모, 손자녀와 사촌 내 혈족 중 본인 제외 2명 이상의 유방암이나 전립선암의 경우.
2.4. 유전자검사 결과 보고
환자 검체를 대행업체에 보내면 대행업체에서 DNA를 뽑고 이를 대상으로 NGS 등의 방법을 통해 유전자검사를 시행한 후 의료진에게 결과보고서를 보내는 것이 관행이다.
1) 결과보고서의 유형
① SNP 번호를 표기한 후 allele type을 기록한 경우.
이는 이상적인 형태의 보고로 임상 의사가 dbSNP에서 그 SNP 번호를 찾아 전술한 방법을 통해 임상적인 의미와 참고문헌을 찾아 도움을 받을 수도 있고 자신의 임상적인 결과를 모아 학회에 발표할 수도 있다.
② 유전자 변이를 식별할 수는 있지만, 임상 의사가 분자생물학적 지식이 있어야 하는 경우.
표 2.
국내 MaXX 회사의 체세포 유전자 돌연변이 보고 예시
보고서의 내용은 다음과 같다.
변이 유전자는 KIT로 대표적인 염기서열 번호(transcript ID)는 NM_000222.2로 총 exon 21개 중 exon 11번에 변이가 위치하며, NM000222.2의 cDNA를 펼치면 1679번째 염기서열이 정상은 T type인데 A로 변이가 관찰됨. 따라서 아미노산 서열 560번 위치에 원래 valine이 aspartate로 변이되는 missense 변이(염기서열의 변화로 아미노산 변이를 초래)이다. 이는 gastrointestinal stromal tumor의 경우 임상적으로 의미 있는 돌연변이로 regorafenib, sunitinib 등이 사용 제시된다(National Institute of Cancer Research, SCV005061462.1). 이런 보고 결과를 바탕으로 임상 의사가 NCBI site에서 정확한 임상의미를 다시 확인할 수 있다. 즉 GenBank (https://www.ncbi.nlm.nih.gov/)에 접속해 NM_000222.2을 입력하면 상기 유전자는 Homo sapiens KIT proto-oncogene, receptor tyrosine kinase (KIT), transcript variant 1, mRNA임을 알 수 있다. dbSNP: rs121913521 이고, 상기 link에 접속하면 10편 이상의 발표된 논문에서 다양한 악성종양에서 체세포 돌연변이에 의한 종양 발생(likely oncogenic)에 관여함과 생식세포 돌연변이(likely pathogenic)에도 관여하고 있다. Site에 있는 “CDS”를 접속해 아미노산 합성에 관여하는 cDNA 염기서열을 구하고, translation된 아미노산 염기서열을 구하면, 결과 변이 [gtt(valine)---> gat(aspartate)]가 있는 부위는 다음과 같다.
정상세포--->1672 aag (lys)gtt(val)gtt(val)gag(glu)gag(glu)ata(ile)
종양세포--->1672 aag (lys)gtt(val)gat(asp)gag(glu)gag(glu)ata(ile)
③ 추적이 가능할 수도 있지만, 유전자 확인이 명확하지 않은 경우
환자가 건강검진을 목적으로 유전자검사를 받고 그 결과 해석을 위해 본원으로 전원된 경우로 환자의 보고서는 다음과 같았다.
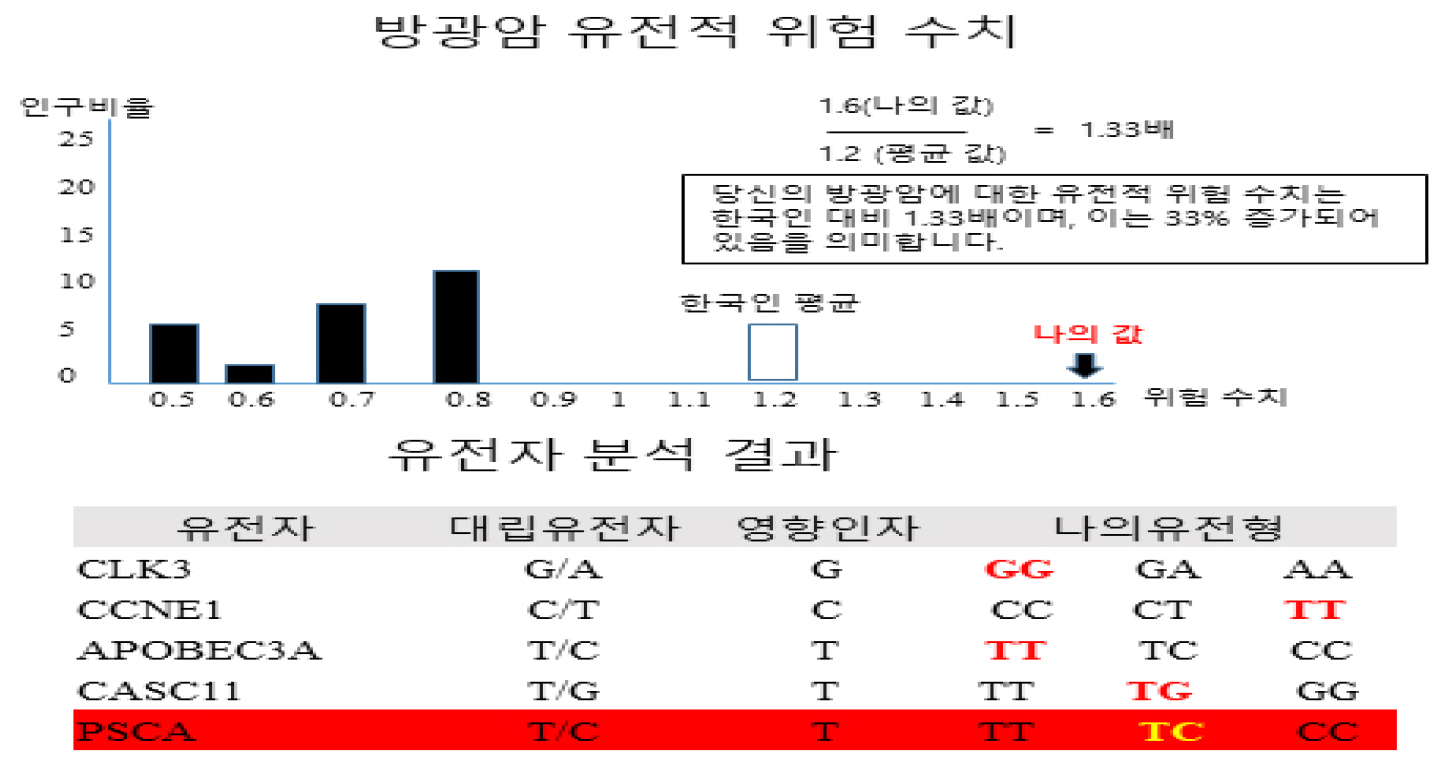
지참한 보고서를 보면 5개의 유전자가 방광암 발생에 관여하고, 이 중 CLK3, APOBEC3A 유전자가 homozygote로 방광암 가능성을 가장 높이고, CASC11, PSCA 유전자는 heterotype으로 중간단계, 그리고 CCNE1은 방광암 억제로 작용한다. 암 발생은 나이 값을 보정이 필요해 결과에 보정한 것을 볼 수 있다.
본례는 생식세포 돌연변이 유전자검사로 유전자 검사회사의 영업비밀에 속하는 것인지 유전자 이름만 알려주고 그 위치 등을 확인할 수가 없는 경우이다. PSCA 유전자의 경우 NCBI site에 7160개의 SNP가 있어 어느 곳의 변이를 지칭하는지 알 수 없다. 저자가 추가적인 논문 등을 조사해 PSCA 유전자 변이는 rs2294008로 추정되지만 확실하지 않다.
④ 유전자 정보 없이 단지 각 질병의 위험도만 알려주는 보고서
분석회사에서 보고한 보고서는 단순하게 각 질병이나 악성종양의 발생 위험도를 Odd ratio로 보고하고 있다. 이러한 보고서를 통해 의료진이 환자에게 줄 수 있는 정보는 거의 없다.
3. 결론
짧은 지면을 통해 유전자검사에 대해 알아보았다. 생식세포 유전자 변이가 있어도 환경을 잘 조절함으로써 질병 발생을 억제할 수 있다는 것은 유전자검사의 장점이지만, 발견 빈도가 매우 낮은 점을 고려한다면 모든 사람을 대상으로 유전자검사를 남용해서는 안 된다. 또한, 적응증이 되어 검사를 시행한 환자의 보고서에 수록된 의미를 잘 해석해 질병 발생억제나 질병의 조기발견에 이바지하여야 할 것이다.
유전정보가 없고 단지 질병 예측도만 알려주는 일부 업체의 보고서는 점쟁이가 점을 치고 그 결과를 믿으라고 강요하는 것으로 그러한 업체와는 거래하지 말아야 한다. 환자의 귀중한 시간과 경비를 고려해 의료진은 유전자 변이결과를 잘 이해하여 환자에게 설명해 주며, 유전자 변이와 관련 있는 특정 질환을 진단할 수 있는 임상적인 검사를 시행하여야 한다. 또한, 환자뿐만 아니라 환자와 관련된 혈족의 질병 상담에도 응용할 수 있어야 한다.