1. 서론
2. 본론
2.1. 1차 치료: 생활습관 교육과 대기관찰요법, 약물치료의 역할과 한계
2.2. 전통적 수술: TURP의 역할 변화와 한계
2.3. 내시경 기반 최소침습 치료법(MIST)의 부상
2.4. First-line Interventional Therapy의 부상
3. 결론
1. 서론
전립선비대증(Benign Prostatic Hyperplasia, BPH)은 연령이 증가할수록 유병률이 높아지는 대표적 노인성 질환인 동시에 진행성 질환으로 경증 환자라도 자연적으로 호전되기보다는 시간이 지남에 따라 증상이 악화되는 경향이 있다 [1,2]. BPH는 전통적으로 증상의 중증도를 주요 기준으로 삼아, 경미한 경우에는 생활 습관 교정과 대기관찰요법(watchful waiting), 중등도 이상의 증상에는 약물치료, 그리고 약물치료의 반응이 없거나 부작용이 있는 중증의 환자 또는 합병증의 위험이 있는 환자에게는 수술적 치료를 고려하는 단계적 접근을 취해왔다 [1].
그러나 경증 환자라도 시간이 지남에 따라 질환이 진행될 위험이 있으며, 대기 관찰 요법은 환자의 불안감과 삶의 질 저하를 초래할 수 있다 [3]. 또한, α-blocker와 5α-reductase inhibitor (5-ARI) 등 주요 약제는 기립성 저혈압, 성기능 장애, 두통, 무력감 등의 전신 부작용 발생 위험을 동반하고, 질환 진행을 완전히 차단하지 못할 뿐만 아니라, 장기 복용 시 순응도가 떨어지며 무엇보다 복용 중단 후 증상 재발을 피할 수 없다는 한계를 지닌다 [4,5]. 무엇보다 환자마다 전립선 크기, 하부요로증상(lower urinary tract symptoms, LUTS)의 양상 및 중증도, 삶의 질 저하 정도, 치료 기대와 목표가 크게 달라, 획일적인 접근보다는 개별 환자의 임상 양상과 선호도를 반영한 맞춤형 치료 전략이 요구된다 [6]. 특히, 정기적인 추적 관찰과 적절한 시점의 치료 개입이 중요하며, 최근에는 약물과 수술 사이의 간극을 메우는 내시경 기반 최소 침습 치료법(Minimally Invasive Surgical Therapies, MIST)에 대한 관심이 커지고 있다. 본 원고에서는 BPH 1차 치료의 한계와 전통적 수술의 변화 양상을 짚어보고, 최근 각광받는 내시경 기반 MIST들의 원리와 임상 근거를 살펴보고자 한다. 또한, 약물 치료와 수술 사이에 위치한 일차 개입 치료(First-line Interventional Therapy) 개념의 부상과 환자별 맞춤 치료의 중요성을 논의하고자 한다.
2. 본론
2.1. 1차 치료: 생활습관 교육과 대기관찰요법, 약물치료의 역할과 한계
BPH 환자의 초기 평가에서 증상이 경미하고 삶의 질에 큰 영향을 미치지 않는 경우에는 생활 습관 교육과 경과 관찰만으로도 관리할 수 있다. 생활 습관 개선에는 취침 전 수분 섭취 제한, 카페인·알코올 절제, 배뇨 습관 개선 등이 포함되며, 이러한 보존적 요법은 부작용이 없다는 장점이 있다.
그러나 BPH는 진행성 질환이므로, 시간 경과에 따른 증상 악화나 급성 요폐(acute urinary retention, AUR)의 위험을 간과할 수 없다. 장기간 경과 관찰군을 대상으로 한 연구에서 상당수의 환자가 결국 적극적인 치료로 전환된 것으로 보고되었으며, 한 연구에서는 감시 대기 중이던 환자의 약 36%가 5년 이내에 수술 등 침습적 치료로 이행한 것으로 나타났다 [7]. 따라서 단순한 경과 관찰을 하더라도 정기적인 추적 관찰과 증상 악화의 징후에 대한 모니터링이 중요하다.
BPH로 인한 LUTS가 일상생활에 불편을 줄 정도로 나타나면 약물 치료를 시작하게 된다. 현재 BPH/LUTS의 약물요법으로 가장 널리 쓰이는 것은 α-blocker와 5-ARI이며, 그 외에 선택적 무스카린길항제나 PDE-5 억제제 등이 환자 상태에 따라 사용된다. α-blocker는 전립선 및 방광경부의 평활근을 이완시켜 비교적 빠른 증상 개선을 유도하지만, 어지러움이나 기립성 저혈압, 역행성 사정 등의 부작용이 문제가 될 수 있다. 5-ARI는 전립선 조직을 위축시켜 장기적으로 전립선 용적을 감소시키고 요폐 또는 수술 필요성을 줄여주는 약제이지만 [2,8,9], 효과 발현까지 수개월이 걸리며, 성기능 감퇴(성욕 감소, 발기저하)나 사정량 감소 등의 부작용이 흔하다. 특히 5-ARI의 복약 순응도는 실제 임상에서 매우 낮으며, 처방 분석 연구에 따르면 1년간 5-ARI 복용을 지속한 환자는 29%에 불과했고, 복합요법의 경우 중도탈락율이 더욱 높았다 [9]. 이처럼 약물치료의 순응도 저하는 약물 효과의 실질적 한계를 초래하며, 결국 약물치료 실패 시에는 침습적 개입이 필요해진다 [2].
또한, 약물 치료는 증상을 완화할 수는 있지만, 근본적인 해부학적 폐색을 제거하지는 못하기 때문에, 전립선 크기가 큰 환자나 폐색 증상이 두드러진 환자에서는 약물만으로 충분한 개선을 기대하기 어렵고, 시간이 지나며 증상이 다시 악화될 수 있다. 이 경우 방광 기능 손상, 반복적인 요로 감염, 요로 결석 등의 합병증 위험도 증가한다. 결국, BPH 관리에 있어 초기부터 질병 진행 위험 인자(예: 전립선 크기, PSA 수치, 증상 점수 등)를 고려하여, 적절한 시점에 보다 적극적인 치료로 전환하는 전략이 요구된다 [10,11]. 이러한 배경에서, 최근에는 약물 치료 단계에서 효과나 순응도가 불충분한 환자에게 조기에 최소 침습적 개입 치료를 고려하는 접근이 대두되고 있다 [6].
2.2. 전통적 수술: TURP의 역할 변화와 한계
증상이 중등도 이상이거나 약물 치료에 반응하지 않는 경우 시행되는 전통적 수술인 경요도 전립선 절제술(transurethral resection of the prostate, TURP)은 오랫동안 표준 치료(gold standard)로 자리매김해 왔다. TURP는 비대된 전립선 조직을 절제하여 방광 출구 폐색(bladder outlet obstruction, BOO)을 해소하는 근본적인 방법이며, 장기적인 증상 개선 효과가 입증되어 있다. TURP 시행 후 환자의 배뇨 증상 점수와 최고 요속(Qmax)은 크게 향상되며, 그 효과가 수년 이상 지속되는 것으로 보고된다 [12,13]. 그러나 TURP는 침습적 외과적 술식으로, 전신 또는 척추 마취에 대한 부담, 출혈 위험, 수액 부하에 따른 저나트륨혈증(TUR 증후군) 등의 합병증 가능성을 동반한다 [12]. 또한, 수술 후 흔하게 발생하는 역행성 사정은 보고에 따라 65~75%까지 발생할 수 있으며, 일부 환자에서는 발기 기능 저하, 일시적 요실금, 요도 협착 또는 방광경부 협착 등의 합병증도 나타날 수 있다 [14,15]. 이러한 합병증 위험과 입원 필요성 때문에 환자들이 수술에 대해 심리적 부담을 크게 느끼며, 실제 임상에서는 수술을 미루거나 기피하려는 경향이 있다 [6,15].
1990년대 이후 BPH 치료에 약물 요법이 도입되고 보편화되면서, 전 세계적으로 TURP 시행률은 꾸준히 감소해 왔다. 특히 중등도 증상의 많은 환자들이 약물로 관리되면서, 예전만큼 일찍 수술적 치료를 고려하지 않게 된 것이다. 더불어 최근 10여 년간 다양한 신기술 기반의 대체 술식들이 등장하여 치료 선택지가 확대되면서, TURP의 상대적 점유율 감소가 두드러진다. 예를 들어 미국 Medicare 인구를 대상으로 한 분석에 따르면, 2013년 BPH 수술의 51%를 차지하던 TURP 비율은 2019년 42%까지 감소한 반면, UroLift와 같은 최소 침습 시술은 2015년 전체의 1.5%에서 2019년 23.7%로 크게 증가하였다 [16]. 그럼에도 불구하고 TURP는 여전히 가장 많이 시행되는 단일 BPH 수술법이며, 특히 전립선 크기가 중간 정도(30~80 mL)이고 증상이 매우 심하거나 BPH로 인한 합병증 위험이 있는 환자에게는 효과적인 해결책으로 고려된다 [16,17]. 최근에는 기존 TURP의 단점을 보완하기 위해 양극성 플라스마 절제술(bipolar TURP), 광선택적 전립선 기화술(photoselective vaporization of the prostate, PVP), 홀렙(holmium laser enucleation of the prostate, HoLEP) 등, 출혈 감소와 안전성 향상을 도모한 다양한 변형 술식들도 도입되었다 [17,18,19]. 그럼에도 TURP로 대표되는 전립선비대증 수술 전반에 내재한 침습성과 수술 부작용에 대한 부담은 완전히 해소되지 않았으며, 이를 극복하기 위한 다양한 내시경 기반 최소 침습 치료(MIST)들이 개발되어 임상에 적용되고 있다 [6,1516,17,18,19].
2.3. 내시경 기반 최소침습 치료법(MIST)의 부상
전통적 수술의 공백을 메우기 위해 최근 각광받는 MIST들은 요도를 통한 내시경적 접근으로 전립선 폐색을 해소하면서도, 조직 손상을 최소화하여 부작용을 줄이는 것을 목표로 한다. 이러한 시술은 대개 국소 마취나 의식하 진정으로 외래 기반에서 시행 가능하며, 입원 기간을 단축하고 회복을 빠르게 한다는 장점이 있다. 또한 일부 기법은 전통적 수술에 비해 성기능 보존 측면에서 우수하여, 성생활 유지가 중요한 비교적 젊은 전립선비대증 환자들에게 매력적인 선택지가 되고 있다 [17,20,21]. 현재 임상에서 사용되거나 연구 중인 대표적인 내시경 MIST로는 수증기를 이용한 경요도 전립선 절제술(transurethral water vapor ablation of the prostate, Rezūm™), 전립선 결찰술(prostatic urethral lift, UroLift®), 전립선 비대증에서 일시적 니티놀 스텐트 삽입술(iTind™ procedure), 워터젯을 이용한 경요도 전립선 절제술(Aquablation®), 약물 코팅 풍선 확장술(drug-coated balloon), 임시 전립선 스텐트 등이 있다 [22]. 각각의 작용 기전과 임상 성과를 아래에 소개한다.
2.3.1. 수증기 이용 경요도 전립선 절제술(Rezūm)
Rezūm은 전립선 실질에 수증기를 주입하여 열에 의한 응고 괴사를 유발하는 최소 침습적 치료이다. 일종의 열 치료로서 2015년 미국 FDA 승인을 받았으며, 전용 장치를 통해 요도 내시경으로 접근한 뒤 전립선 선종에 가는 바늘을 삽입하여 고온의 수증기를 분사한다. 수증기는 조직 내에서 응축되며 열 에너지를 방출해 국소적인 세포 파괴를 일으키고, 이후 해당 조직은 체내 면역 작용에 의해 서서히 흡수되어 제거된다. Rezūm 시술은 통상 국소 마취하에 약 10~15분 내에 완료되며, 시술 후 일시적으로 도뇨관을 3~7일 유치하여 초기 부종이 가라앉을 때까지 소변 배출을 돕는다 [22,23,24].
Rezūm의 가장 큰 장점은 시술의 간편성과 성기능 보존에 있다. 조직 절제가 아닌 고열 수증기를 제한된 범위에 주입 방식이므로 주변 신경과 구조물에 손상을 주지 않으며, 임상 연구들에서는 사정 기능의 변화 없이 증상 개선이 달성된 것으로 보고되었다 [25]. 5년간 추적한 REZŪM II 무작위 대조시험에서 Rezūm 시술군은 위약 대조군 대비 LUTS 지표인 국제 전립선 증상 점수(IPSS)가 45% 감소하고, 삶의 질(QoL) 점수도 유의하게 개선되었으며, 최대 요속(Qmax)은 49% 향상되었다 [26]. 해당 연구에서 5년간 재치료율은 4.4%로 매우 낮게 유지되었고, 성기능 면에서도 시술로 인한 발기부전이나 사정 장애는 발생하지 않았다. 다른 장기 보고들에서도 Rezūm 시술 후 4년 시점까지 개선된 증상 점수와 요속이 유지되었으며, 성기능 설문지에서도 사정 기능의 유의한 변화는 관찰되지 않았다 [22,23,24]. 이러한 근거를 바탕으로 Rezūm은 현재 중등도 크기(약 30~80 mL)의 전립선을 가진 환자에서 유효한 치료 옵션으로 인정받고 있다. 다만 전립선 용적이 80 mL 이상으로 매우 큰 경우나, 요로 감염이 있는 경우, 또는 인공 괄약근이나 음경 보형물이 삽입된 상태에서는 적용이 어렵다. 또한 시술 직후 수주 간 배뇨통, 빈뇨, 혈뇨 등의 일시적인 자극 증상이 흔히 발생할 수 있다. 그럼에도 불구하고 Rezūm은 약물 치료에 비해 단기간에 더 큰 증상 개선을 보이며, 약물로 충분한 효과를 보지 못한 환자들에게는 비수술적 대안으로서 가치가 크다 [27].
2.3.2. 전립선결찰술(Prostatic Urethral Lift, UroLift®)
UroLift는 전립선의 양쪽 측엽 조직을 영구적인 이식형 결찰사로 묶어 당겨줌으로써 요도를 넓혀 방광출구 저항을 낮춰주는 치료법이다. 내시경을 Urolift delivery device를 삽입한 뒤, 전립선 요도의 좌우측에 스테인리스 스틸/니티놀 합금 재질의 임플란트를 삽입하여 polyethylene terephthalate (PET) monofilament suture의 장력으로 전립선 조직을 인·고정한다 [22]. 쉽게 말해 전립선 내부에 작은 커튼 걸이를 설치해 좁아진 통로를 양옆으로 열어주는 개념이다. 시술 시간은 1시간 이내이며, 출혈이 거의 없어 대부분 도뇨관을 유치하지 않고도 당일 자가배뇨가 가능하다. 조직 절제나 열 손상을 가하지 않기 때문에 방광경부, 괄약근, 사정관 등의 구조를 그대로 보존할 수 있고, 시술 후에도 정상적인 사정 기능이 유지된다는 점이 큰 장점이다 [22,28,29,30,31].
UroLift 시술군은 단기간(수주 이내)에도 증상 점수 개선이 관찰될 정도로 효과 발현이 빠르며 [21,22], 무작위 대조군 연구(L.I.F.T. Study)에서도 시술 3개월 후 평균 AUA 증상 점수(IPSS와 동일한 7문항)가 22.3±5.8점에서 11.1±7.7점으로 절반 가까이 개선되었고, 평균 Qmax도 4.0 mL/s 증가하여 최대 5년까지 유지되었다 [32]. 성기능 측면에서는 위약군과 비교하여 발기 기능이나 사정 기능에 유의한 변화가 없었고, 오히려 일부 환자에서는 성 만족도가 향상되었다는 보고도 있다 [31]. TURP와 직접 비교한 연구에서는 증상 개선 효과는 Urolift 시술군이 열등하지 않았고, 사정 기능 보존율이 월등히 높고 수술 후 회복이 빨라 조기 퇴원 및 일상 복귀에 유리한 것으로 나타났다 [29,30].
UroLift의 한계로는 재치료율이 다소 높다는 점이 지적된다. 이식된 결찰사는 영구적으로 남지만 전립선비대증은 지속적으로 진행될 수 있기 때문에, 장기적으로 증상이 재발하거나 추가 치료가 필요한 경우가 있다. 5년 추적 결과 약 13%의 환자가 추가적인 BPH 치료를 받은 것으로 보고되었으며 [32,33], 이 중 일부는 임플란트를 유지한 상태에서 약물 치료를 병행하거나, 결찰사를 제거하고 TURP와 같은 수술적 치료를 시행하기도 하였다. 또한 전립선 중앙엽(median lobe)이 돌출된 환자에서는 요도 리프트 단독으로는 증상 개선이 어려울 수 있다. 하지만 이러한 단점을 감안하더라도, UroLift는 성기능을 중시하는 환자층이나 마취 고위험군에서 안전하게 시행할 수 있는 효과적인 치료로 자리 잡았다. 시술의 편의성과 즉각적인 효과, 그리고 낮은 부작용 프로파일 덕분에 전 세계적으로 빠르게 보급되고 있으며, 앞서 언급했듯 미국 내 BPH 시술 중 차지하는 비율이 급증하고 있다 [10].
2.3.3. 전립선 비대증에서 일시적 니티놀 스텐트 삽입술(iTind™ procedure)
iTind (temporarily implanted nitinol device)는 니티놀 합금으로 제작된 장치를 전립선 요도에 삽입하여 5~7일 동안 유지함으로써 방광경부 및 전립선 요도를 영구적으로 넓히는 비영구적 임플란트 기법이다 [그림 1]. 특수한 3차원 꽃봉오리 모양의 니티놀 와이어 구조물을 접은 상태로 14Fr 카테터를 통해 요도 방광 내시경을 이용하여 전립선 요도에 위치시킨 후 펼쳐지게 한다 [34,35,36]. iTind 장치는 체내에서 서서히 펼쳐지며, 세 개의 와이어 지지대(strut)가 전립선 요도 벽을 지속적으로 눌러 압박 자국을 남긴다. 이 압박 효과로 방광경부와 전립선 요도에 영구적인 삼각형 모양의 새로운 통로가 형성되는데, 이는 외과적으로 전립선절개술(Transurethral incision of the prostate, TUIP)에서 5시, 7시, 12시 방향으로 절개를 가하는 것과 유사한 효과를 얻을 수 있다 [그림 2]. 일정 시간이 지난 후 국소 마취하에 간단히 장치를 제거하면 전립선 요도의 내강이 넓어져 하부 요로 증상의 개선을 기대할 수 있다 [22,37].
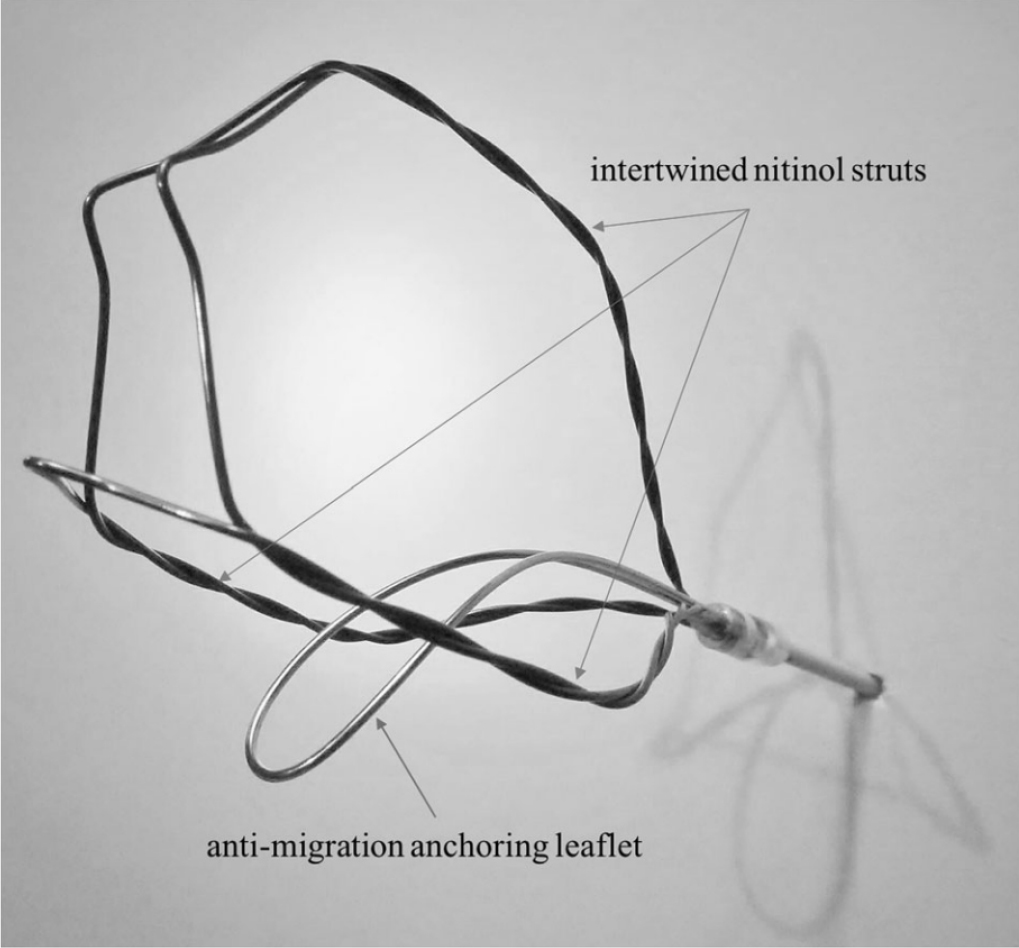
그림 1.
iTIND 기기의 구조. 이 기기는 세 가닥의 니티놀 스트럿(strut)과 고정용 리플렛(leaflet)으로 구성되어 있다. Adapted from [38] Amparore et al., Prostate Cancer Prostatic Dis. 2021;24(2):349–357.
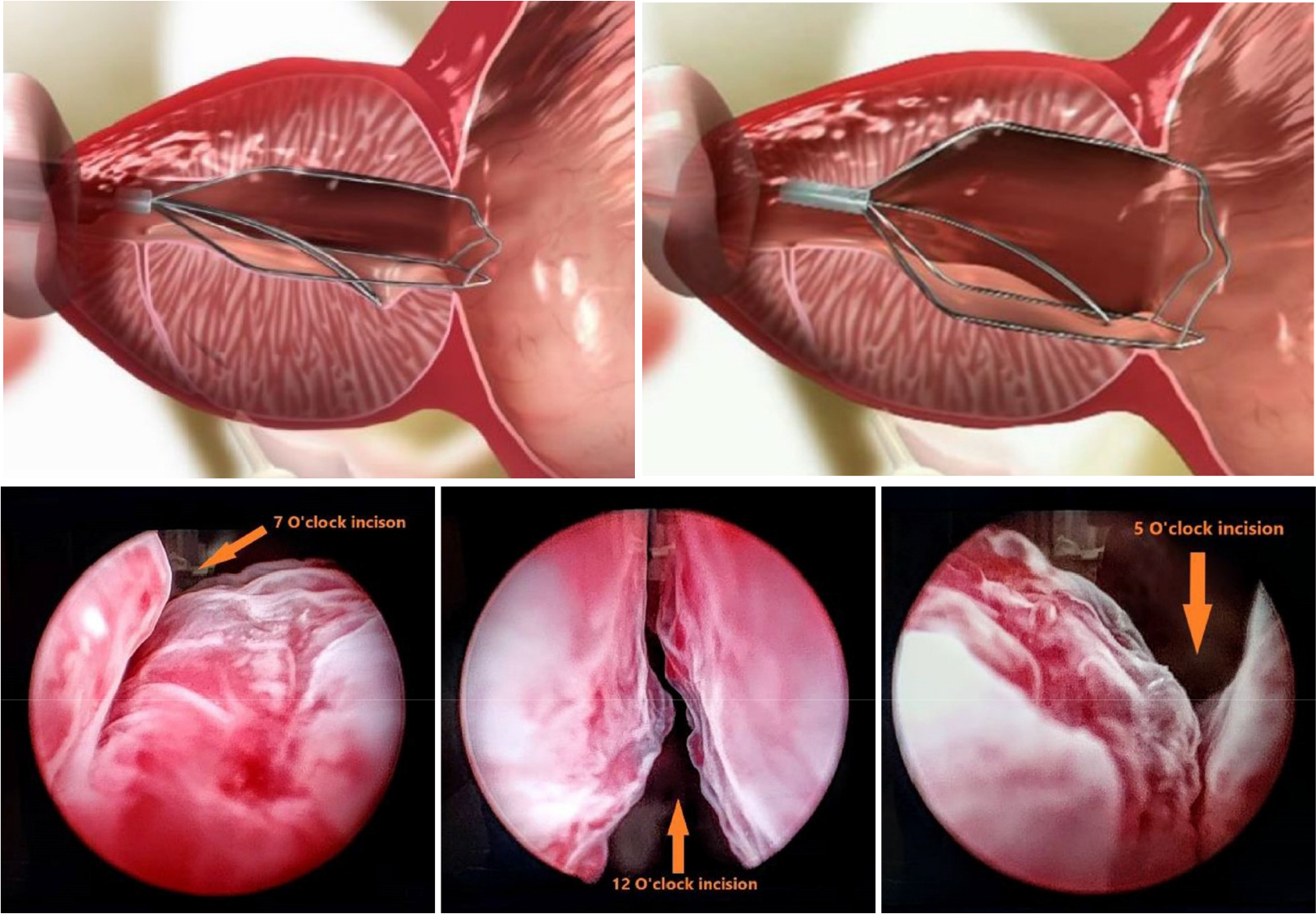
그림 2.
압축 상태(crimped configuration)의 iTIND 기기 구조와 기기 제거 후 내시경 이미지. 전립선 요도에 형성된 7시, 12시, 5시 방향의 절개선을 관찰할 수 있다. Adapted from [36] Kadner et al., World J Urol. 2020;38(12):3235–3244.
iTind는 비영구 장치로, 시술 후 약 1주일 이내의 단기간 장치 삽입만으로 효과를 발휘하므로, 체내 이물에 대한 장기 합병증 위험이 적고 필요 시 반복 시술이나 다른 치료로의 전환이 용이하다. 무엇보다 영구적인 조직 절제나 열 손상을 주지 않기 때문에 시술로 인한 영구적인 부작용이 최소화된다 [22,38]. iTind 시술 후 12개월 시점에 IPSS는 평균 9.25±6.49점 감소하였고, 최대 요속은 3.52±5.24 mL/s 증가하여 대조군 대비 유의한 개선을 보였으며, 삶의 질 점수(QoL)도 1.90±1.74점 호전되었다 [36]. 또한 성기능 검사상 발기 및 사정 기능에 유의미한 변화는 없었다 [38]. 2년 추적 연구에서도 초기 호전된 LUTS 지표가 유지되었고, 사정 및 성기능의 손실 없이 효과가 지속되었다는 보고가 있다 [35]. 약 2년 내 재치료가 필요한 경우는 5% 내외로 보고되었으며 [33], 이는 주로 전립선 용적이 큰 일부 환자에서 증상 재발로 인해 TURP 등으로 전환된 사례였다.
iTind의 적응증으로는 전립선 크기가 중등도 이하이며 약물 치료에 순응하기 어려운 환자, 또는 성기능 보존을 최우선으로 원하는 환자 등이 제시된다. 시술 과정에서 별도의 에너지원이 필요 없기 때문에 출혈이나 염증 외의 합병증이 드물며, 기계적 요도 확장 효과로 인해 시술 직후 증상 개선이 빠르게 나타날 수 있다. 다만 장치가 요도 내에 있는 5~7일 동안은 불편감, 빈뇨, 절박뇨, 일시적인 배뇨 곤란 등이 발생할 수 있으므로, 그 기간을 견딜 수 있는 환자여야 한다. 또한 일정 기간 후 반드시 장치를 제거해야 하므로 추적이 어려운 환자에게는 부적합하다 [22,33]. iTind는 유럽을 중심으로 상용화되어 사용되고 있으며, 미국 FDA 승인도 획득하여 점차 임상 근거가 축적되고 있다. iTind는 가역적이면서도 효과가 지속될 수 있는 시술로서, 향후 BPH 치료의 중요한 축이 될 수 있을지 주목받는 MIST 중 하나이다.
2.3.4. 워터젯을 이용한 경요도적 전립선 절제술(Aquablation®)
Aquablation은 초음파 유도하에 고압의 식염수 물줄기(water jet)를 이용하여 전립선 조직을 제거하는 기술로, 2015년 처음 소개되었다. 이 시술은 AquaBeam© (PROCEPT Biorobotics, Redwood Shores, CA, USA) 시스템을 통해 이루어진다. 수술자는 실시간 경직장 초음파 영상으로 전립선의 절제 범위를 계획하고, 자동화된 water jet 분사 장치가 장착된 24Fr 내시경 핸드피스를 요도를 통해 삽입하여 설정된 범위만큼 water jet으로 조직을 선택적으로 절제한다 [39]. 이처럼 초음파 영상을 통해 목표 범위를 정하고 자동으로 절제 작업을 수행하기 때문에, 주변 조직 손상을 최소화하면서 정밀한 절제가 가능하다. 레이저나 전류를 사용하지 않으므로 열 손상이 없고, 자동 절제 시스템 덕분에 수술자의 숙련도에 따른 편차도 적다는 장점이 있다. 다만 실제 임상에서는 추가적인 지혈이 필요하고 시술에 어느 정도 경험이 요구된다. 시술 시간은 전립선 크기에 따라 다르나, water jet 절제 단계는 10분 이내로 매우 신속하다. 일반적으로 시술 후 도뇨관을 수일간 유지하고, 마취는 척추 마취, 경막외 마취 또는 전신 마취가 필요하다 [22,39,40].
Aquablation은 중간 크기부터 거대 전립선까지 폭넓게 적용 가능하며, 기존 TURP 대비 효과 면에서도 비견할 만한 임상 자료가 축적되고 있다. 가장 주목할 만한 연구는 30~80 mL 전립선을 대상으로 Aquablation과 TURP를 비교한 무작위 임상인 WATER 연구이다. 5년 추적 결과, 두 군 모두 IPSS가 크게 감소하여 증상 개선 효과는 유사하였으나(Aquablation군 15.1점 감소 vs TURP군 13.2점 감소, P=0.27), 전립선 용적이 큰 하위군(50~80 mL)에서는 Aquablation이 TURP 대비 추가적인 증상 개선 효과를 보였다(IPSS 개선 폭 3.5점 더 큼) [40,41,42]. 최대 요속 개선률은 Aquablation군이 125%로, TURP군의 89%보다 높았고, 사정 기능 보존률 측면에서도 Aquablation이 우수했다. 5년간 시술 관련 역행성 사정 발생률은 Aquablation이 7%에 불과한 반면 TURP는 25%에 달해, 전통적 절제술 대비 사정 기능 유지에 큰 이점을 보였다. 재치료율도 Aquablation이 연 1% 수준으로 낮아, 5년 누적 재시술 및 재약물치료 비율이 TURP 대비 51% 적었다 [41]. 또한 80~150 mL 거대 전립선을 대상으로 단일군으로 시행한 WATER II 연구에서도 2년 시점에 IPSS 17점 개선, Qmax 8.7 mL/s 증가 등의 유의한 효과가 나타나, 크기가 큰 전립선에도 적용 가능함을 시사하였다 [43,44].
Aquablation의 강점은 자동화된 술기로 인한 효율성과 일관성, 그리고 우수한 성기능 보존이다. 특히 성생활을 유지하고자 하는 비교적 젊은 환자나, 전립선이 매우 커서 HoLEP이나 개복 수술을 고민해야 하는 환자에게 매력적인 대안이 될 수 있다 [22]. 또한 술기 자체가 비교적 단순화되어 수술자의 학습 곡선이 완만할 것으로 기대된다. 그러나 단점으로는 전용 장비 도입 비용이 높고, 장비 운용을 위한 별도의 공간 확보 및 마취과 전문의에 의한 마취가 필요하다는 점이 있다. 또한 시술 중 출혈 가능성을 배제할 수 없으며, 실제 초기 연구에서 Aquablation군의 수혈률이 TURP보다 다소 높게 보고되기도 했다 [45].
Aquablation은 아직 국내외에서 장기 추적 데이터가 충분하지 않으며, AquaBeam© 시스템 자체가 고가이고 국민건강보험 급여 적용이 되지 않아 치료비 부담이 크다. 또한 water jet을 이용한 조직 절제 방식은 다른 MIST보다 출혈 위험이 높고 마취가 반드시 필요하여, 실제 임상에서는 비용 대비 효과와 안전성 측면에서 여전히 논의가 필요한 실정이다. 이러한 이유로 국내에서는 아직 Aquablation의 보급이 제한적이며, 기존 표준 술식(TURP)이나 다른 MIST와 비교해 명확한 우위를 점했다고 보기 어렵다. 향후 더 많은 연구와 경험이 축적되어 안전성, 경제성, 효능이 충분히 검증되지 않는 한, 실질적인 보편 치료로 자리 잡기까지는 다소 시간이 필요할 것으로 보인다.
2.3.5. 약물 코팅 풍선카테터(Drug-Coated Balloon: Optilume® BPH 시스템)
Optilume® BPH 시스템의 주된 시술 목적은 전용 확장 풍선을 이용하여 전립선 요도의 anterior commissure에 절개를 가한 후, 양측엽(lateral lobe) 사이의 공간을 확보하고, paclitaxel을 전립선 선종 부위에 전달하여 재유합(refusion) 및 지속적 성장을 방지하는 것이다 [그림 3]. 2023년 미국 FDA 승인을 받은 Optilume® BPH 카테터 시스템은 두 개의 풍선 카테터로 구성되며, 첫 번째 전확장용 풍선으로 전립선 요도를 물리적으로 넓힌 뒤, 두 번째 약물(paclitaxel) 코팅 풍선이 동일 부위에 팽창되어 확장 효과를 유지하면서 약물을 조직에 방출한다 [46,47]. Paclitaxel은 세포 증식 억제 효과가 있어 손상 부위의 과도한 반흔 형성을 막아주며, 풍선 확장 후 요도가 다시 좁아지는 것을 방지하는 역할을 한다.
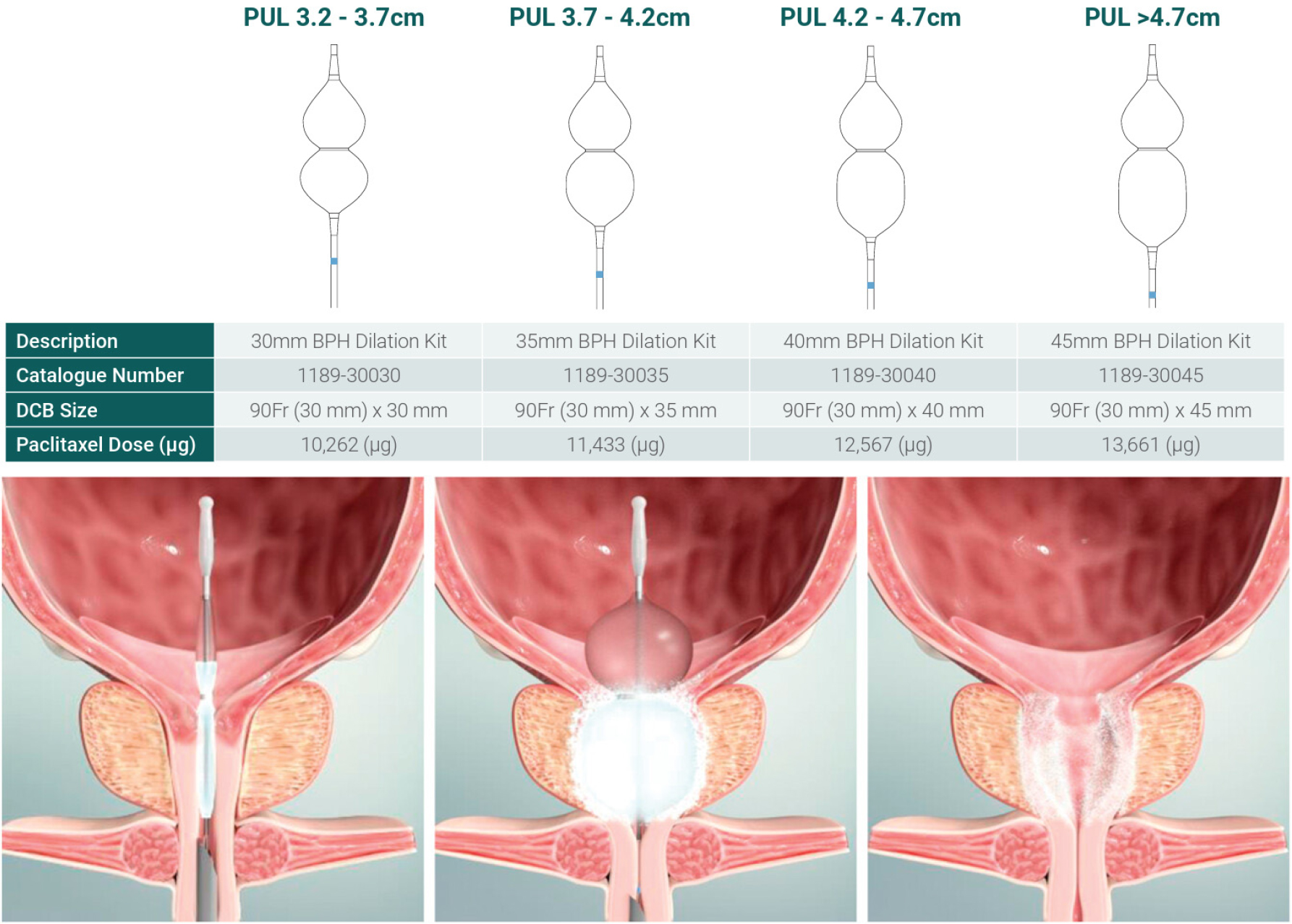
그림 3.
Optilume® BPH 카테터 시스템. 이 시스템은 전립선 요도를 확장하는 비코팅 예비 확장용 풍선과 paclitaxel을 전달하는 약물 코팅 풍선(DCB)으로 구성된다. Adapted from LABORIE Medical Technologies Corp. website (https://www.laborie.com/product/optilume-for-bph) and [49] Kaplan et al., J Urol. 2023;210(3):500–509.
시술 과정은 비교적 간단하여 국소 마취하에 당일 외래 기반 시술로 진행된다. Optilume® BPH 시스템은 코팅되지 않은 예비 확장용 풍선 카테터(uncoated predilation catheter)와 약물 코팅 풍선 카테터(drug-coated balloon, DCB), 총 2종의 카테터로 구성된다. Optilume® BPH DCB는 모두 90F 직경을 가지며, 치료 길이는 30 mm부터 45 mm까지 네 가지로 제공된다 [그림 3]. 시술 전에는 경직장 초음파(transrectal ultrasound)로 전립선 요도의 길이를 측정한 뒤, 그에 따라 개별 전립선에 맞는 카테터 크기를 선택한다. 시술은 20F 경성 방광경(rigid cystoscope)으로 시야를 확보한 후, 코팅되지 않은 예비 확장용 카테터를 전립선 요도에 직접 위치시키는 것으로 시작된다. 카테터 샤프트에 표시된 마킹은 장치 배치를 정밀하게 조정하는 데 도움이 되며, 시술 내내 방광경을 통해 이를 확인할 수 있다. 이후 예비 확장용 풍선을 약 1분간 팽창시켜 anterior commissure 부위를 절개 및 확장하고, 이어서 DCB를 같은 방식으로 삽입하여 약 5분간 팽창함으로써 전립선 요로상피에 paclitaxel을 전달한다. 시술 후에는 일반적으로 도뇨관(Foley catheter)을 2일 정도 유지한다 [47].
이러한 과정을 통해 Optilume® BPH 시스템 시술은 전립선 요도의 확장 효과를 극대화하고, 약물 방출에 따른 재협착 예방 효과까지 기대할 수 있다. 특히 이중 로브 풍선 설계를 적용하여 카테터 이탈을 최소화하고 시술 과정에서의 안정성을 높였다는 점에서, 기존 팽창 시스템과 차별화된 강점으로 알려져 있다. 시술 후 도뇨관은 1~2일 이내에 제거 가능하며, 환자는 즉시 일상생활로 복귀할 수 있다. 임상적 효과는 풍선 확장으로 인한 즉각적인 BOO 완화로 빠르게 나타난다. 2021년 발표된 PINNACLE 임상시험 1년 결과에 따르면, 약물 코팅 풍선 시술군에서 평균 IPSS 점수는 23.0±5.4에서 10.9±6.6으로 크게 개선되었고, 최대 요속(Qmax)은 평균 8.7±2.1 mL/s에서 19.0±10.3 mL/s로 증가하였다 [47]. 이러한 Qmax 개선 폭은 동일 기간의 다른 MIST들과 비교해 우수한 수준으로, 일시적 요도 확장의 즉각적인 효과와 paclitaxel의 지속 효과를 함께 기대할 수 있음을 시사한다. 최근 2년 추적 결과에서도 전체 환자의 67.5%가 추가 치료 없이 IPSS 30% 이상 개선을 유지해 내구성을 입증하였다 [46]. 또한 약물 방출 풍선 치료는 주변 조직 손상이 거의 없어 발기나 사정 기능에 대한 부작용이 드물며, 전신 약물 노출이 미미해 전신적 부작용 우려도 낮은 편이다.
약물 코팅 풍선 요법의 제한점으로는 이 시술이 비교적 새롭게 개발되어, 장기적인 효과와 안전성에 대한 데이터가 아직 제한적이라는 점이 있다. 현재까지는 2년 추적 결과가 양호하지만, 5년 이상의 장기 추적 데이터 확보가 필요하며, paclitaxel에 대한 국소 조직 반응과 잠재적 영향에 대한 지속적인 모니터링이 요구된다. 그럼에도 불구하고 Optilume® BPH 시스템은 비수술적이면서도 효과적인 요도 확장 방식으로, 기존 수술이나 MIST조차 어려운 고령 환자, 또는 내과적 중증 동반 질환 환자에게 새로운 선택지로 주목받고 있다. 또한 절차가 간단하고 환자 순응도가 높아 일부에서는 1차 치료로도 활용 가능하다는 전망이 있으며, 실제로 해외에서는 임상 적용이 시작되고 있다 [6,22].
2.3.6. 전립선 스텐트 – 일시적 요도 스텐트
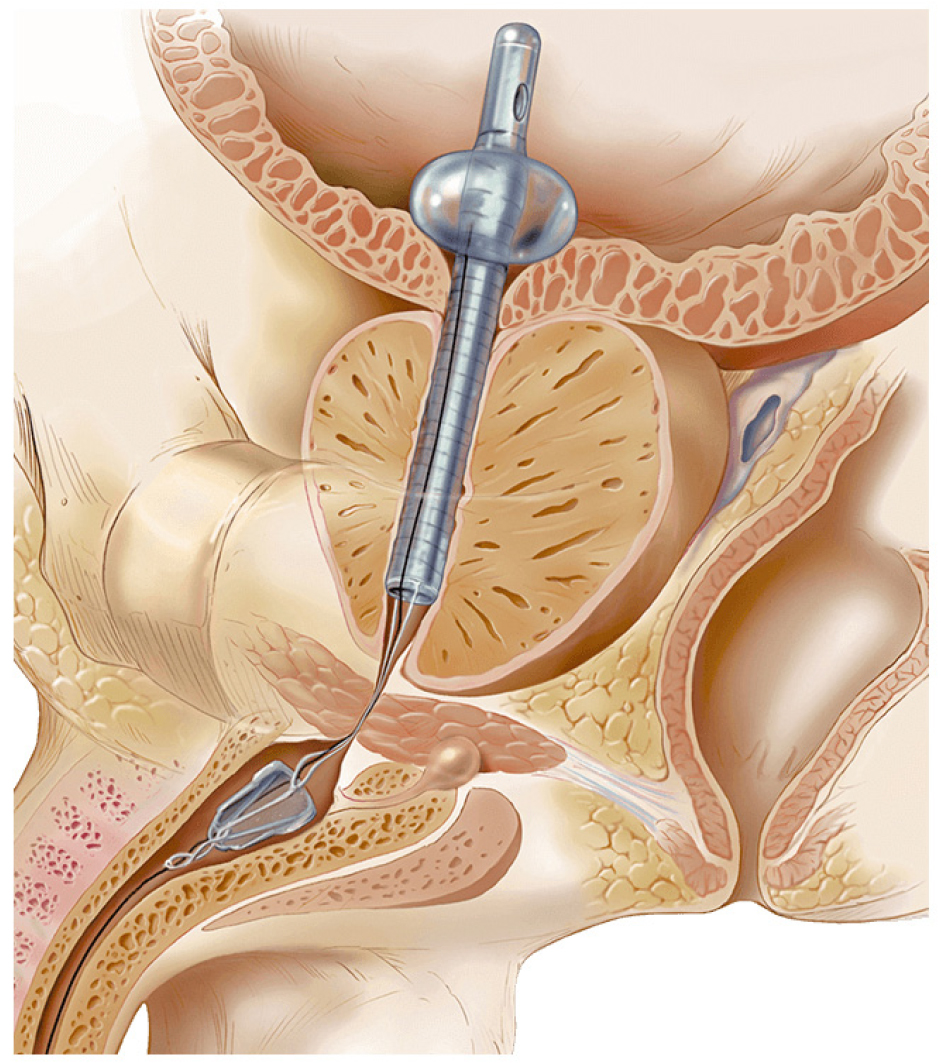
일시적 전립선 스텐트는 전립선 요도에 일정 기간 동안만 삽입되어 요도 개방을 유지하는 방식의 치료법이다. 가장 잘 알려진 기기는 Spanner™ prostatic stent로, 이는 요도 괄약근 바로 위에서 전립선 요도까지를 지지해주는 작은 T자 형태의 튜브이다 [그림 4]. Spanner™ prostatic stent는 국소 마취하에 요도에 삽입되어 통로를 확보하며, 최대 1개월간 체내에 두었다가 제거하거나 필요 시 교체할 수 있다. 주로 만성 요폐로 도뇨관에 의존하지만 수술은 어려운 환자에게 도뇨관의 대안으로 사용되며, 또는 TUMT(경요도 열치료) 등 시술 후 일시적 보조 장치로 활용되어 왔다 [48].
일시적 스텐트의 목적은 전립선 폐색을 즉각적으로 해소하여 자연 배뇨를 가능하게 하는 데 있다. 도뇨관을 장기간 유치하면 불편감과 감염 위험이 높고 삶의 질이 저하되지만, 스텐트는 요도를 개방하면서도 환자의 불편이 적어 환자의 편의성이 높은 편이다. 실제 Spanner™ prostatic stent 삽입 시 배뇨압이 감소하고 최대 요속은 유의하게 증가하며, 잔뇨량도 크게 줄어든다 [49]. 한 연구에서는 스텐트를 3개월에 걸쳐 교체 사용한 결과, 대상 환자의 74%가 성공적으로 도뇨관 없이 자가 배뇨를 유지했고, 평균 최대 요속은 11.2 mL/s, IPSS는 7.5점으로 양호한 배뇨 상태를 보였다 [50]. 일시적 스텐트 삽입은 고령이거나 수술이 불가능한 환자에서 즉각적인 요배출 확보에 유의미한 치료 옵션으로 평가된다.
그러나 임시 스텐트는 합병증과 불편감으로 인해 널리 사용되지는 못하고 있다. 대표적인 문제는 스텐트의 이탈 또는 이동, 요석 형성 및 감염이다 [50]. 스텐트가 체내에 오래 머무를수록 표면에 침전물이 쌓여 자극 증상이 발생할 수 있으며, 방광 내로 스텐트가 빠지거나 반대로 요도 쪽으로 밀려나오는 경우도 있다. 또한 일부 환자는 스텐트 삽입 후에도 배뇨통이나 빈뇨가 지속되어 조기 제거를 원하기도 한다. 실제 보고에 따르면, 수술이 불가능한 환자에서 스텐트를 사용한 경우 63%에서 통증이나 요정체로 인해 스텐트를 제거해야 했다 [48].
따라서 이러한 임시 스텐트는 환자 선택이 매우 중요하며, 방광 수축 기능이 충분하고 감염 관리가 가능한 환경에서 제한적으로 활용되고 있다. 최근에는 디자인 개선을 통해 부작용을 줄이기 위한 연구가 진행되고 있으며, 일부 새로운 개념의 스텐트(Zenflow Spring System 등)도 개발되고 있다 [51]. 임시 전립선 스텐트는 영구적인 이식물 없이도 폐색을 완화한다는 ‘개념 증명(proof of concept)’의 의미를 가지며, 향후 소재공학의 발전과 함께 보완·발전될 수 있는 분야로 평가된다.
2.4. First-line Interventional Therapy의 부상
앞서 살펴본 최소 침습 시술의 발전으로 BPH 치료 패러다임에 새로운 개념이 대두되고 있다. 바로 일차 개입 치료(First-line Interventional Therapy, FIT) 개념으로, 이는 기존의 ‘증상이 심하지 않으면 약물 치료부터 시작’이라는 틀에서 벗어나, 초기 단계부터 MIST와 같은 시술적 치료를 고려하자는 접근이다 [6]. 이러한 개념은 BPH 환자들의 실제 요구와 기존 치료의 한계에서 출발하였다. 많은 환자들이 수술의 부작용과 위험성 때문에 침습적 치료를 미루고 싶어하며, 반면 약물 치료는 장기간 복용에 따른 부작용과 낮은 만족도로 인해 중도에 포기하는 경우가 흔하다. FIT는 바로 이 간극을 메워줄 치료로서, 약물을 장기간 투여하지 않고도 신속한 증상 완화를 이루고 부작용을 최소화하며, 회복이 빨라 환자의 삶의 질을 조기에 개선할 수 있는 MIST를 조기에 시행하는 것이 핵심이다.
현재 이용 가능한 MIST들은 앞서 살핀 바와 같이 각기 장단점이 있지만, 이상적인 FIT의 요건을 모두 충족하는 것은 아닐 수 있다. 이상적인 일차 개입 치료란 외래에서 짧은 시간 내에 시행 가능하고, 빠르게 효과가 나타나며, 합병증이 극히 적고, 충분한 지속 기간 동안 재치료 없이 지낼 수 있으며, 향후 필요 시 더 침습적인 치료로의 전환도 자유로운 형태일 것이다. 예를 들어 Rezūm이나 UroLift 등은 입원 없이 시술 가능하고 성기능에도 영향이 적어 FIT의 취지에 부합하지만, 일부 환자에서는 효과가 불충분하거나 재치료가 필요할 수 있다. 반면 TURP와 HoLEP (Holmium Laser Enucleation of the Prostate) 등은 효과와 지속성 면에서는 뛰어나나, 초기 침습성이 크기 때문에 전통적으로 일차 치료가 아닌 최후의 수단으로 고려되어 왔다. FIT는 환자 개개인의 특성과 기대치에 따라 다양한 치료 옵션의 우선순위를 재배열하는 접근이라고 할 수 있다. 예를 들어, ‘약물 복용을 원치 않고 빠른 개선을 원하는 50대 환자’라면 초기부터 UroLift와 같은 시술을 선택할 수 있고, ‘약물로 효과를 보지 못한 60대 환자’에게는 Rezūm을 조기에 권유하여 증상 악화를 예방할 수 있다. 이러한 접근은 기존의 단계적 치료 알고리즘을 유연하게 재구성함으로써 환자 만족도를 높이고, 방광 기능 악화와 같은 질병 진행을 조기에 차단할 수 있다는 잠재적 이점이 있다.
실제로 최근 FIT 개념을 제창하는 문헌들이 등장하고 있다. Elterman과 Kaplan 등 [6]은 기존의 ‘약물 치료 후 수술’이라는 고식적인 체계에서 벗어나, 초기부터 최소 침습 시술을 적극적으로 고려함으로써 환자들에게 더 나은 삶의 질과 방광 건강을 장기적으로 제공할 수 있다고 강조하고 있다. 현재의 MIST들이 FIT의 가능성을 보여주지만, 그 효과와 근거는 아직 충분히 확립되어 있지는 않다. 향후 환자 중심 결과(patient-centered outcomes)를 최우선으로 하여 외래에서 안전하게 시행할 수 있는 새로운 기술이 개발될 필요가 있으며, 끊임없는 기술 발전을 통해 FIT는 BPH 치료에서 약물과 수술 사이의 과도하게 넓은 간극을 메우는 새로운 패러다임으로 자리 잡을 수 있을 것이다. 이러한 흐름은 앞으로의 임상 연구 방향에도 영향을 주게 되며, 축적된 근거는 다시 한 번 BPH 치료 패러다임의 변화를 이끌 것으로 기대된다.
3. 결론
BPH는 진행성 질환이며, 환자마다 전립선의 크기와 형태, 증상의 종류 및 심각도, 그리고 치료에 대한 기대와 목표가 다양하다. 이에 따라 모든 환자에게 동일한 치료를 적용하기보다는, 각 환자의 질병 진행 위험 인자(전립선 용적, PSA 수치, 증상 점수 등)와 개인적 가치관 및 선호도를 철저히 평가하고 파악하는 것이 중요하다. 약물 치료에서 최소 침습 시술, 나아가 수술적 치료에 이르기까지 다양한 치료 옵션을 조합하여, 환자의 삶의 질을 최적화하고 합병증을 최소화하는 전략이 요구된다. 성생활을 중요시하는 환자에게는 성기능 보존에 유리한 시술을 고려하고, 반대로 증상 개선의 최대치를 원하거나 재치료를 피하고자 하는 환자에게는 보다 근본적인 절제술을 조기에 적용하는 식의 개별화된 접근이 바람직하다. 최신 트렌드로 부상한 다양한 최소 침습 수술(MIST)과 일차 개입 치료(First-line Interventional Therapy, FIT) 개념은 이러한 개인별 접근을 가능케 하는 BPH 치료 전략이다. 앞으로 각 치료법의 장기 효과와 최적 대상 환자군이 추가 연구를 통해 명확해지고, 환자와 의사가 충분한 정보를 바탕으로 공동 의사결정을 할 수 있게 된다면, BPH 관리에 있어 ‘일률적인(one-size-fits-all) 치료’는 점차 자리를 잃고 환자 맞춤형 치료 시대가 더욱 각광받게 될 것이다. 궁극적으로 다양한 치료 옵션 중 환자의 기대와 목표에 부합하는 최선의 선택지를 함께 찾아가는 것이 BPH 치료의 핵심임을 우리 비뇨의학과의사들은 항상 기억해야 한다.