1. 서론
고강도 초음파 집속술은 1940년대 Lynn 등이 시험적 고강도 초음파 집속술에 대하여 발표한 것을 시초로, 이미 70년 정도의 역사를 가지고 있다 [1]. 하지만 실제로 고강도 초음파 집속술이 임상에서 널리 쓰이게 된 것은 최근 20년 이래의 일이다. 고강도 초음파 집속술은 1999년 프랑스 회사인 Edaps tms가 첫번째 경직장 고강도 초음파 집속술 기계를 개발하여 첫번째 임상 사용이 시작되게 되었다. 당시 그 기계는 두 개의 초음파 발생기가 하나의 프로브에 융합되어 있어 영상 촬영과 고강도 초음파 집속을 위한 치료 초음파 발생이 동시에 가능한 형태로 설계되었다. 프랑스에서는 2003년 국소 전립선암의 치료에 대해서 허가가 이루어졌고 이후 2014년에는 프랑스 보건복지부에서 일부 환자들에 대해서 보험 적용이 시행되게 된다. 미국에서는 SonaCare medical이라는 회사가 역시 2004년 경직장 고강도 초음파 집속술 기계를 출시하였으며, 2014년 Edaps tms와 SonaCare medical은 같이 전립선 조직 파괴에 대하여 FDA 승인을 받게 된다. 고강도 초음파 집속술은 최근 새롭게 혜성처럼 등장한 신기술은 아니지만, 적극적 관찰 요법 등의 보존적 치료에 대한 관심이 높아짐에 따라 함께 점차 주목을 받고 있다.
2. 본론
1867년 Theodor Billroth에 의하여 처음으로 회음부 절개를 통한 근치적 전립선 절제술이 시행 이후, 근치적 수술은 전립선암 치료에 있어서 대표적인 치료법이었다 [2]. 그러나 전립선 절제술은 요실금, 발기부전 등의 합병증으로 인하여 환자들의 삶의 질에 중대한 영향을 주는 한계가 있었으며, 한편 전립선 특이 항체의 개발 및 사용으로 인하여 환자들의 병기는 이전에 비하여 좀더 초기에 발견되는 일이 많아지게 되었다. 특히 글리슨 점수 6점의 전립선암 경우에는 거의 전이를 하지 않고 진행이 느린 것으로 알려지면서 이러한 저위험도 환자에서 수술이나 방사선 치료 등의 적극적 치료를 지양하고 대신 관찰을 하는 새로운(특이한) 개념의 ‘적극적 관찰 요법’이 등장하게 되었다. 최근 캐나다의 Klots 등의 연구에 따르면 적극적 관찰 요법은 10년 암특이생존률을 98.1%로 매우 우수한 결과를 보여주었다 [3]. 그러나 적극적 관찰 요법도 지속적으로 반복적인 전립선 조직검사를 받아야 하기 때문에 환자들에게 주는 불편은 여전히 무시할 수 없는 것이 사실이다. 이러한 배경 속에서 고강도 초음파 집속술 역시 애초 개발 당시에는 근치적 전립선 절제술 또는 방사선 치료를 대체하기 위한 Whole gland treatment을 목적으로 하였으나, 최근에는 Partial or Focal gland treatment로 좀더 보존적인 치료 방법으로 개념이 변화하게 되었다.
2.1. 고강도 초음파 집속술의 기전
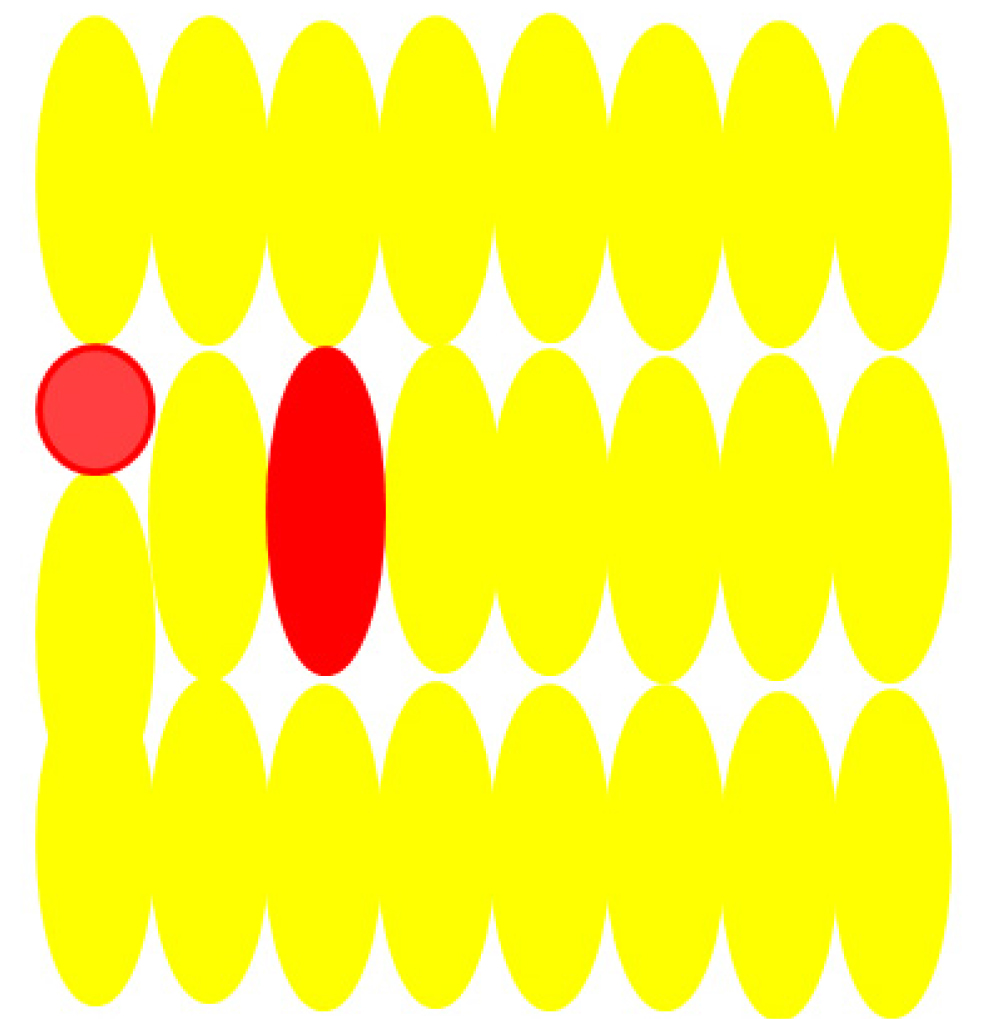
현재의 고강도 초음파 집속술은 Thermal or non-thermal effects 두 개의 효과를 이용한다. 초음파 에너지를 고강도로 집중을 시킴으로 해서 조직 온도를 80도 이상으로 끌어올릴 수 있으며, 이러한 고열은 직접적 조직의 손상을 가져오게 되어 결국 coagulation necrosis에 빠지게 된다. Non-thermal effects는 고강도 초음파 집속술 당시 발생하는 microbubble들이 끌어오르는 진동 현상에 의해서 발생하게 되며, 이러한 mircrobubble은 세포벽의 비가역적인 손상을 초래하게 되어, 세포의 괴사를 초래하게 된다 [그림 1]. 고강도 초음파 집속술은 애초에 초음파를 집중시켜야 하기 때문에, 매우 작은 영역만 한번의 초음파 방출로 태워버릴 수 있다. 기계에 따라서 이 한번에 태울 수 있는 영역의 크기는 다를 수 밖에 없는데, 주로 5 mm에서 1 cm의 크기 정도이다(focal points). 따라서 넓은 면적을 태워버리기 위해서는 고강도 초음파 집속술은 하나의 focal point에 해당하는 영역을 태우고, 프로브를 이동하여 옆에 다시 인접하여 다른 focal point를 태우는 작업을 반복하는 방식으로(focal point라는 점을 나란히 쌓아서) 넓은 면적을 ablation할 수 있게 된다. 현재 출시되어 있는 모든 기계는 이러한 작동 원리를 가지고 있으며, focal point 사이의 남거나 치료 되지 않고 넘어가는 공간이 없도록 focal point마다 약간의 중첩되는 영역을 설정하여 세팅되는 것으로 알려져 있다. 그러나 고강도 초음파 집속술 도중에는 프로브가 계속 회전하고 위아래로 움직이게 되고, 또한 직장의 연동 운동이 존재하기 때문에 전립선은 따라서 같이 움직이게 된다. 이러한 움직임은 focal point와 focal point 사이의 혹시라도 ablation이 되지 않은 skipped lesion의 위험성을 가져오게 되고, 해당 가능성은 술 후의 재발 또는 잔존암으로 이어질 수 있는 위험성이 있다 [그림 2]. 또한 현재 초음파 기반의 고강도 초음파 집속술 기기들은 조직의 온도를 정확하게 측정하는 방법이 없으며, 따라서 원하는 정도의 ablation이 실제 이루어졌는지 술 중에 feedback을 받을 수 있는 방법이 없다. 최근 개발되고 있는 MRI-guided HIFU machine들은 thermometry software들이 내장되어 있어 좀더 정확한 치료가 가능하도록 발전되고 있는 양상이다.
2.2. 고강도 초음파 집속술의 임상 결과
고강도 초음파 집속술은 술자의 선택에 따라서 전체 전립선을 ablation하거나 일부 전립선만을 ablation하는 다양한 치료의 선택의 가능성이 있기 때문에 일률적으로 결과를 비교하기 어려운 특징이 있다. 현재는 이러한 고강도 초음파 집속술의 종류를 Whole gland ablation, Partial gland ablation, Focal gland ablation 이렇게 세가지 정도로 분류 하는 것이 대부분이다.
2.2.1. Whole gland ablation
초기에는 거의 모든 고강도 초음파 집속술은 Whole gland ablation으로 이루어졌다. Thuroff 등은 704명을 대상으로 Whole gland ablation 을 시행한 결과 10년 암특이 생존률 99%, 무전이 생존률을 95%로 우수한 결과를 보여주었으며, 전체적인 부작용은 16%에서 나타나지만 술자의 경험이 축적되면서 점차 줄어드는 양상을 보고하였다 [4]. 한편 Ganzer 등이 발표한 논문은 Whole gland ablation 시행받은 538명의 환자를 분석한 결과, 암특이 사망률은 low risk group에서 0%, intermediate group에서 5.7%, high risk group에서 15.4%로 보고하였다 [5]. 프랑스의 Crouzet등은 1002명의 많은 환자를 대상으로 whole gland ablation을 시행한 결과, 10년 암특이 생존률은 97%로 보고하였으며, 세부적으로 보면 low risk group에서 99%, intermediate group에서 98%, high risk group에서 92%로 기존의 radical prostatectomy에 견주어 볼만한 결과를 보고하였다 [6]. Crouzet의 연구에서 수술 후 요실금은 5%의 환자에서 발생하였다.
2.2.2. Hemi-gland ablation
더 우수한 기능적 결과를 가져오기 위해서, 고강도 초음파 집속술은 점차 Whole gland treatment에서 Focal treatment로 진화를 하게 된다. Rischamann등은 111명의 환자를 대상으로 partial gland ablation을 시행하고 1년 뒤 전립선 조직검사를 시행한 결과, 86%의 환자에서 치료한 부분에서는 암이 발견되지 않았으며 발기 기능은 수술전의 78%에서 정상화되는 것을 확인하였다 [7]. 요실금은 3%의 환자에서 나타났으며, 이는 zero pad를 기준으로 한 결과였다. Feijoo 등은 71명의 환자를 대상으로 partial gland ablation을 시행하였으며, 역시 1년째 추적 조직검사에서 25.4%의 환자에서 잔존암 또는 재발암이 존재하는 것을 발견하였다 [8]. Ganzer 등의 다른 연구는 54명을 대상으로 전향적 연구를 시행하였으며, 1년째 조직검사에서 26.5%의 환자가 치료한 부분에서, 28.6%의 환자는 치료하지 않은 영역에서 잔존암이 나타났다는 결과를 발표하기도 하였다 [9].
3. 고강도 초음파 집속술의 한계와 미래
고강도 초음파 집속술은 비침습적이며 기존의 치료에 비하여 기능적 결과(요실금, 발기부전)에 대하여 더 우수한 성적을 보여주는 희망적인 부분은 있으나, 전립선암이 실제로는 60%이상의 환자에서 1개 이상 발생하는 근원적 특성으로 볼 때, 한계점이 존재하는 것이 사실이다. 또한 whole gland ablation을 시행하는 것에 따라 부작용이 증가하기 때문에 단순 발기기능만으로 무조건 고강도 초음파 집속술이 환자의 삶의 질에 우수하다는 결론은 매우 성급하며, 조금 더 정확한 비교 연구가 필요하다. 고강도 초음파 집속술을 포함한 국소 치료는 어떠한 환자를 대상으로 시행하는 지가 가장 중요한데, 아직까지도 전립선암의 유무를 정확히 예측하는 영상학적 검사의 부재, 전립선 조직검사의 한계점 등으로 인하여 어려운 점이 있다. 현재의 가이드라인은 low risk group과 intermediate risk group의 환자들의 경우, Active surveillance를 받거나 Surgery or radiation therapy를 받는, 어떻게 보면 극단적인 두 부류의 치료법 사이에서 선택을 하도록 되어 있는데, 앞으로의 기술의 발달, 그리고 surveillance technique들의 재정립 등을 통하여 미래에는 Focal therapy 또는 고강도 초음파 집속술이 surveillance와 active treatment의 중간 단계로서 어느 정도 자리를 잡을 가능성은 상당히 높다고 생각된다.